 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试从电极电势[如φ(Sn2+/Sn)、φ(Sn4+/Sn2+)及φ(O2/H2O)],说明为什么常在SnCl2溶液中加入少量纯锡粒
试从电极电势[如φ(Sn2+/Sn)、φ(Sn4+/Sn2+)及φ(O2/H2O)],说明为什么常在SnCl2溶液中加入少量纯锡粒以防止Sn2+被空气(O2)氧化。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试从电极电势[如φ(Sn2+/Sn)、φ(Sn4+/Sn2+)及φ(O2/H2O)],说明为什么常在SnCl2溶液中加入少量纯锡粒以防止Sn2+被空气(O2)氧化。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试从电极电势[如φ(Sn2+/Sn)、φ(Sn4+/Sn2+…”相关的问题
更多“试从电极电势[如φ(Sn2+/Sn)、φ(Sn4+/Sn2+…”相关的问题
试从电极电势[如φ(Sn2+/Sn)、φ(Sn4+/Sn2+)及φ(O2/H2O)],说明为什么常在SnCl2溶液中加入少量纯锡粒以防止Sn2+被空气(O2)氧化。
(1)化学反应的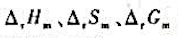 和电池电动势及电极电势值的大小,哪些与化学反应方程式的写法无关?
和电池电动势及电极电势值的大小,哪些与化学反应方程式的写法无关?
(2)为何H2S水溶液不能长期保存?
(3)能否用铁制容器盛放CuSO4溶液?
(4)配制SnCl2溶液时,为防止Sn2+被空气中氧所氧化,通常在溶液中加入少许Sn粒,为什么?
(5)铁溶于过量盐酸或过址稀硝酸,其氧化产物有何不同?
(6)为何金属Ag不能从稀H2SO4或盐酸中置换出H2,,却能从氢碘酸(HI)中置换出H2?
A.加入Sn粒
B.加入Fe屑
C.通入H2
D.以上三项均可
(A) SnCl2水解 (B) SnCl2被氧化 (C) SnCl2歧化 (D) SnCl2被还原
已知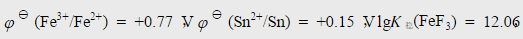 。通过计算说明下列氧化还原反应能否发生,若能发生写出其化学反应式。(设有关物质的浓度为1.0mol·dm-3)
。通过计算说明下列氧化还原反应能否发生,若能发生写出其化学反应式。(设有关物质的浓度为1.0mol·dm-3)
(1)向 溶液中加入SnCl2。
溶液中加入SnCl2。
(2)向FeCl3溶液中加入NaF,然后再加SnCl2。