 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
铜的相对原子质量为63.55,密度为8.96g/c。①计算铜的点阵常数和原予半径。②测得Au的摩尔分数为40%的Cu-Au固溶
铜的相对原子质量为63.55,密度为 。①计算铜的点阵常数和原予半径。②测得Au的摩尔分数为40%的Cu-Au固溶体点阵常数a=0.3795nm,密度为
。①计算铜的点阵常数和原予半径。②测得Au的摩尔分数为40%的Cu-Au固溶体点阵常数a=0.3795nm,密度为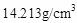 ,计算说明它是什么类型的固溶体。
,计算说明它是什么类型的固溶体。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
铜的相对原子质量为63.55,密度为 。①计算铜的点阵常数和原予半径。②测得Au的摩尔分数为40%的Cu-Au固溶体点阵常数a=0.3795nm,密度为
。①计算铜的点阵常数和原予半径。②测得Au的摩尔分数为40%的Cu-Au固溶体点阵常数a=0.3795nm,密度为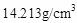 ,计算说明它是什么类型的固溶体。
,计算说明它是什么类型的固溶体。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“铜的相对原子质量为63.55,密度为8.96g/c。①计算铜…”相关的问题
更多“铜的相对原子质量为63.55,密度为8.96g/c。①计算铜…”相关的问题
Fe-Mn-c合金中,Mn和c的质量分数为12.3%及1.34%,它是面心立方固溶体,测得点阵常数a=0.3642nm,合金密度为7.83g/cm3,计算说明它是什么类型固溶体。
Zn原子的摩尔分数为3%Zn的Cu-Zn合金固溶体,铜的原子半径为0.128nm,Zn的原子半径为0.133nm。假设点阵常数随Zn原子增加呈线性变化,求这个合金的密度。
纯铝晶体为面心立方点阵,已知铝的相对原子质量Ar(Al)=26.97,原子半径r=0.143nm,求铝晶体的密度。