 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用电解沉积的办法分离Cd2+和Zn2+,已知H2在Cd上的超电势为0.48V,在Zn上的超电势为0.70V,溶液中的Cd2+和Zn2+
用电解沉积的办法分离Cd2+和Zn2+,已知H2在Cd上的超电势为0.48V,在Zn上的超电势为0.70V,溶液中的Cd2+和Zn2+浓度皆为0.1mol/kg。(已知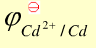 =-0.403V,
=-0.403V,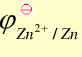 =-0.763V,离子的活度系数均为1,溶液的pH保持中性。)通过计算回答下面的问题:
=-0.763V,离子的活度系数均为1,溶液的pH保持中性。)通过计算回答下面的问题:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“用电解沉积的办法分离Cd2+和Zn2+,已知H2在Cd上的超…”相关的问题
更多“用电解沉积的办法分离Cd2+和Zn2+,已知H2在Cd上的超…”相关的问题

1.jpg) 假设电解过程中保持溶液的pH=7,析出的H2(g)压力为100kPa。
假设电解过程中保持溶液的pH=7,析出的H2(g)压力为100kPa。















