 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25℃时,Ka(HAc)=1.75×10-5。计算该温度…”相关的问题
更多“已知25℃时,Ka(HAc)=1.75×10-5。计算该温度…”相关的问题
A.4.30×10-4mol·dm-3
B.6.25×10-4mol·dm-3
C.1.06×10-3mol·dm-3
D.5.68×10-2mol·dm-3
在0.10mol/L的HAc溶液中,加入NaAc使NaAc浓度为0.10mol/L。计算该溶液的pH和HAc的离解度。
计算pH=4.00时,浓度为0.1000mol·L-1的HAc溶液中,HAc和Ac-的分布分数和平衡浓度。
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω。已知该电导池常数Kcell=36.7m-1,试求该条件下HAc的解离度和解离平衡常数。
已知:
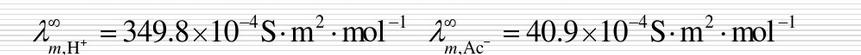
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离平衡常数Ksp约为______;将该溶液稀释后,其pH将变______,解离度α将变______,其将______。
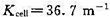 ,试求该条件下HAc的解离度和解离平衡常数。
,试求该条件下HAc的解离度和解离平衡常数。