 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度时8.0mol SO2和4.0mol O2在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压
某温度时8.0mol SO2和4.0mol O2在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压力分别为300kPa和220kPa。利用上述实验数据计算该温度时反应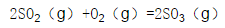 的平衡常数和SO2的转化率。
的平衡常数和SO2的转化率。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度时8.0mol SO2和4.0mol O2在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压力分别为300kPa和220kPa。利用上述实验数据计算该温度时反应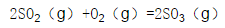 的平衡常数和SO2的转化率。
的平衡常数和SO2的转化率。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某温度时8.0mol SO2和4.0mol O2在密闭容器中…”相关的问题
更多“某温度时8.0mol SO2和4.0mol O2在密闭容器中…”相关的问题
某温度时,8.0mol S02和4.0molO2在密闭容器中反应生成SO3气体,测得起始和平衡时,系统的总压力分别为300kPa和220kPa。试求该温度时反应 的平衡常数和SO2的转化率。
的平衡常数和SO2的转化率。
某温度时,8.0molSO2(g)和4.0molO2(g)在密闭容器中进行反应生成SO3(g),反应为2SO2(g)+O2(g)==2SO3(g),测得起始时和平衡时(温度不变)系统的总压力分别为300kPa和220kPa。计算上述反应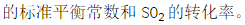
实验测得SO2氧化为SO3的反应,在1000K时,各物质的平衡分压为p(SO2)=27.7kPa、p(O2)=40.7kPa、p(SO3)=32.9kPa。计算该温度下反应2SO2(g)+O2(g)====2SO3(g)的平衡常数Kp。
某温度下,在体积为2L的密闭容器中加入PCl3和Cl2,发生化学反应:PCl3(g)+Cl2(g)═PCl5(g)。反应前 n(PCl3)=4.0mol 反应前 n(Cl2)=2.0mol 平衡时 n(PCl5)=0.80mol 请回答:
(1)该反应PCl3的转化率______.(2)此温度下,该反应的化学平衡常数K=______.
在温度T时,将NH2COONH4(s)置于抽空的容器中,当反应
 达平衡时,测得总压力为p,则反应的标准平衡常数
达平衡时,测得总压力为p,则反应的标准平衡常数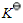 =______。
=______。