 更多“计算下列电池在25℃时的电动势(忽略活度系数):”相关的问题
更多“计算下列电池在25℃时的电动势(忽略活度系数):”相关的问题
,E^θ(CIlAgCIlAg)=0.2222V,电池电动势的温度系数为:
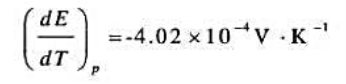
(1)写出电池反应;
(2)计算反应的标准平衡常数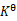 ;
;
(3)计算电池反应的可逆热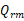 ;
;
(4)求溶液中ZnCl2的平均离子活度因子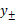 。
。
测得下列电池的电动势为0.792V(25℃);
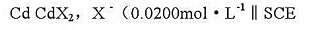
已知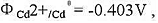 忽略液接电位,计算CdX2的Ksp.(CdX2为镉的难溶盐)
忽略液接电位,计算CdX2的Ksp.(CdX2为镉的难溶盐)
25℃,电池“




在25℃时用下列电池
标准氢电极|待测pH试液||饱和甘汞电极测得如下一系列溶液的电动势,试根据电动势计算溶液的pH。
当电池的电动势 E = 0 V时()
A电池反应中,反应物的活度与产物的活度相等
B电池反应中,反应物的活度与产物的浓度相等
C正、负极的电极电势相等
D正、负极的标准电极电势相等
电池Pb|PbSO4(s)|NaSO4·10H2O饱和溶液|HgSO4(s)|Hg(1)在25℃时的电动势为0.9647V,电动势的温度系数为1.74×10-4V·K-1。
利用表7.4.1(在教材中)的数据计算下列电池在25℃时的电动势。
Cu|CuSO4(b1=0.01mol·kg-1)||CuSO4(b2=0.1mol·kg-1)|Cu
电池:(—)Pt|Sn2+,Sn4+溶液||NCE(),在25℃时,电池电动势为0.0728V。计算溶液中cSn4+/cSn2+的值。(已知:
25℃时,下列电池的电动势E=1.1365V,电动势的温度系数
Ag|AgCl(s)|HCl(a±=0.6)|Cl2(g,100kPa)|Pt
已知25℃时Ag(s)与Cl2(g)的标准熵分别为42.55J·K-1·mol-1及223.07J·K-1·mol-1。试求AgCl(s)25℃时的


 如果结果不匹配,请
如果结果不匹配,请 
















