 更多“计算25℃时纯水的电导率。已知25℃时。”相关的问题
更多“计算25℃时纯水的电导率。已知25℃时。”相关的问题
第4题
25℃时测得SrSO4饱和溶液的电导率为1.482×10-2S·m-1,在该温度下纯水的电导率是1.5×10-4S·m-1,计算SrSO4的溶
25℃时测得SrSO4饱和溶液的电导率为1.482×10-2S·m-1,在该温度下纯水的电导率是1.5×10-4S·m-1,计算SrSO4的溶解度。
第5题
25℃时测得SrSO4饱和溶液的电导率为1.482×10-2S·cm-1,在该温度下纯水的电导率是1.5×10-4S·cm-1,计算SrSO4在
25℃时测得SrSO4饱和溶液的电导率为1.482×10-2S·cm-1,在该温度下纯水的电导率是1.5×10-4S·cm-1,计算SrSO4在水中的溶解度。
第6题
已知25℃时。纯水的电导率K=5.50×10-6S·m-1,无限稀释时H+和OH-的摩尔电导率分别为349.82×10-4及198.0×10-4S·m
已知25℃时。纯水的电导率K=5.50×10-6S·m-1,无限稀释时H+和OH-的摩尔电导率分别为349.82×10-4及198.0×10-4S·m2·mol-1,纯水的密度P=997.07kg·m-3。试求水的离子积为若干?
第7题
已知25℃时水的离子积Kw=1.008×10-14,NaOH,HCl和NaCl的分别等于0.024811S·m2·mol-1,0.042616S·m2·mol-1,0.01
已知25℃时水的离子积Kw=1.008×10-14,NaOH,HCl和NaCl的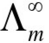 分别等于0.024811S·m2·mol-1,0.042616S·m2·mol-1,0.012645S·m2·mol-1。求25℃时纯水的电导率。
分别等于0.024811S·m2·mol-1,0.042616S·m2·mol-1,0.012645S·m2·mol-1。求25℃时纯水的电导率。
第8题
已知25℃时AgBr(s)的溶度积Ksp=6.3×10-13。利用表7.3.2(在教材中)中的数据计算25℃时用绝对纯的水配制AgBr饱和
已知25℃时AgBr(s)的溶度积Ksp=6.3×10-13。利用表7.3.2(在教材中)中的数据计算25℃时用绝对纯的水配制AgBr饱和水溶液的电导率,计算时要考虑水的电导率。
第9题
求25℃时纯水的电导率。已知25℃时水的离子积Kw=1.008×10-14,NaOH、HCl和NaCl的Λm∞分别等于0.024 811
S.m2.mol-1、0.042 616S.m2.mol-1和0.012 645S.m2.mol-1。
点击查看答案


 如果结果不匹配,请
如果结果不匹配,请 
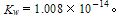 ,纯水的电导率为k,试计算纯水的电导率。
,纯水的电导率为k,试计算纯水的电导率。















