 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
N2O5(g)→N2O4(g)+(1/2)O2(g)为一级反应。在25℃时,反应速率常数为0.0010min-1。同温度下产物N2O4能分解成NO2(g
N2O5(g)→N2O4(g)+(1/2)O2(g)为一级反应。在25℃时,反应速率常数为0.0010min-1。同温度下产物N2O4能分解成NO2(g),并很快达平衡:N2O4(g) 2NO2(g),反应平衡常数
2NO2(g),反应平衡常数
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
N2O5(g)→N2O4(g)+(1/2)O2(g)为一级反应。在25℃时,反应速率常数为0.0010min-1。同温度下产物N2O4能分解成NO2(g),并很快达平衡:N2O4(g) 2NO2(g),反应平衡常数
2NO2(g),反应平衡常数
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“N2O5(g)→N2O4(g)+(1/2)O2(g)为一级反…”相关的问题
更多“N2O5(g)→N2O4(g)+(1/2)O2(g)为一级反…”相关的问题
某温度下反应2NO(g)+O2(g)===2NO2(g)的速率常数k=8.8×10-2mol-2.dm6.s-1,已知反应对O2来说是一级反应,则对NO为________________级反应,反应的速率方程为________________;当反应物浓度均为0.05 mol.dm-3时,反应的速率是________________。
N2O5分解反应N2O5→2NO2+1/2O2是一级反应,已知其在某温度下的速率常数为4.8×10-4s-1。(1)求t1/2;(2)若反应在密闭容器中进行,反应开始时容器中只充有N2O5,其压力为66.66kPa,求反应开始后10秒和10分钟时的压力。
蔗糖催化水解
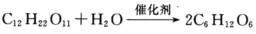 是一级反应。在25℃速率常数为5.7×10-5s-1。问: (1)浓度为1mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
是一级反应。在25℃速率常数为5.7×10-5s-1。问: (1)浓度为1mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
温度为500K时,某理想气体恒容反应的速率常数 则此反应用压力表示的反应速率常数kp=().
则此反应用压力表示的反应速率常数kp=().
蔗糖催化水解是一级反应,在25℃时,若其速率常数为5.7×10-5s-1。问: (1)浓度为1 mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
醋酸酐的分解是一级反应,其反应速率常数k与温度T有如下关系:lg(k/s—1)=12.0414—7.537×103/(T/K)欲使此反应在10min内转化率达到90%,应如何控制温度?
阿司匹林的水解为一级反应。100℃时的速率常数为7.92d-1,活化能为56.5kJ·mol-1。计算37℃下阿司匹林水解20.0%所需的时间。