 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知液态松节油萜的消旋作用是一级反应,在458K和510K时速率常数分别为k(458K)=2.2×10-5min-1和k(510K)=3.07
已知液态松节油萜的消旋作用是一级反应,在458K和510K时速率常数分别为k(458K)=2.2×10-5min-1和k(510K)=3.07×10-3min-1。试求反应的实验活化能Ea,以及在平均温度时的活化焓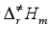 、活化熵
、活化熵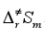 和活化Gibbs自由能
和活化Gibbs自由能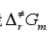 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知液态松节油萜的消旋作用是一级反应,在458K和510K时速率常数分别为k(458K)=2.2×10-5min-1和k(510K)=3.07×10-3min-1。试求反应的实验活化能Ea,以及在平均温度时的活化焓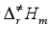 、活化熵
、活化熵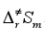 和活化Gibbs自由能
和活化Gibbs自由能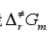 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知液态松节油萜的消旋作用是一级反应,在458K和510K时…”相关的问题
更多“已知液态松节油萜的消旋作用是一级反应,在458K和510K时…”相关的问题
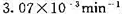 。试求反应的实验活化能
。试求反应的实验活化能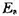 ,以及在平均温度时的活化焓
,以及在平均温度时的活化焓
双环戊烯单分子气相热分解反应,在483K时的速率常数k(483K)=2.05×10-4s-1,在545K时的速率常数k(545K)=1.86×10-2s-1。已知kB=1.38×10-23J·K-1,h=6.626×10-34J·s。
试计算:
(1)反应的活化能Ea
(2)反应在500K时的活化焓和活化熵
 308 K时,
308 K时,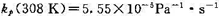 .若A(g)和B(g)的原子半径和摩尔质量分别为
.若A(g)和B(g)的原子半径和摩尔质量分别为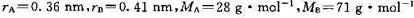 .试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓
.试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓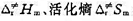 和活化Gibbs自由能
和活化Gibbs自由能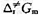 .
.
某基元反应A(g)+B(g)→P(g),设在298K时的速率常数kp(298K)=2.777×10-5Pa-1·s-1;308K时,kp(308K)=5.55×10-5Pa-1·s-1。若A(g)和B(g)的原子半径和摩尔质量分别为rA=0.36nm,rB=0.41nm,MA=28g·mol-1,MB=71g·mol-1。试求在298K时,
1)
该反应的概率因子
P
;
(2)
反应的活化焓
△
r
*
H
m
,活化熵
△
r
*
S
m
和活化
Gibbs
自由能
△
r
*
G
m
。

298K时,某化学反应加了催化剂后,其活化熵和活化焓比不加催化剂时分别下降了10J·mol-1·K-1和10kJ·mol-1,试求在加催化剂前后两个速率常数的比值。
A.表观活化能很大
B.活化熵有绝对值较大的负值
C.活化熵有较大的正值
D.活化焓有绝对值较大的负值
298K时有两个级数相同的基元反应A和B,设两个反应的活化焓相同,但速率常数却不同,kA=10kB,试计算两个反应的活化熵的差值。
已知青霉素G的分解反应为一级反应,37℃时其活化能为84.8kJ·mol-1,指前因产A为4.2×1012h-1,求37℃时青霉素G分解反应的速率常数?