 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(
在一定的温度下,为使电池
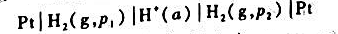
的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(填>,<,=.)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定的温度下,为使电池
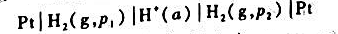
的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(填>,<,=.)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H…”相关的问题
更多“在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H…”相关的问题
由标准氢电极与饱和甘汞电极(SCE)组成电池:
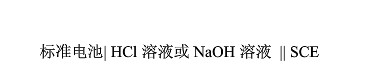 上述电池,在HCl溶液中测得电动势为0.276V;在NaOH溶液测得电动势为1.036V;在100mL HCl及NaOH的混合溶液中测得电动势为0.958V。计算这100mL的混合溶液中,HCl及NaOH溶液各有多少毫升?(φSCE=0.2412V)
上述电池,在HCl溶液中测得电动势为0.276V;在NaOH溶液测得电动势为1.036V;在100mL HCl及NaOH的混合溶液中测得电动势为0.958V。计算这100mL的混合溶液中,HCl及NaOH溶液各有多少毫升?(φSCE=0.2412V)
若氢电极为一缓冲溶液时,测得电池电动势为0.427V,求缓冲溶液的pH。
A.P1=P2
B.P1>P2
C.P1
D.P1和P2都可以取任意值
A.电极发生极化作用时,阳极电势一定升高,阴极电势一定降低
B.因为扩散是不可逆过程,所以浓差电池一定是不可逆电池
C.电极的极化作用一定会导致原电池的电动势降低
D.电池中只要有电流通过,该电池就一定不是可逆电池
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
由标准氢电极和镍电极组成原电池。若c(Ni2+)=0.010mol·dm-3时,电池的电动势为0.316V,其中镍为负极,计算镍电极的标准电极电势。
电池反应: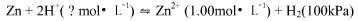 ,其中c(Zn2+)=1.00mol·L-1,P(H2)=100kPa,298.15K时测其电池的电动势为+0.460V,求氢电极溶液中的pH值是多少?
,其中c(Zn2+)=1.00mol·L-1,P(H2)=100kPa,298.15K时测其电池的电动势为+0.460V,求氢电极溶液中的pH值是多少?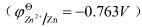
反应:Zn(g)+2H+(mol·L-1)====Zn2+(1.0mol·L-1)+H2(100kPa),测得该电池反应的电池电动势为0.46V,求氢电极中溶液的pH。已知(Zn2+/Zn)=-0.76V。