 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
温度为25℃、压强为1.013x10^5Pa的1mol刚性双原子分子理想气体,经等温过程体积膨胀至原来的3倍。(普适气体常量R=8.31J.mol^-1.K^-1)(1)计算这个过程中气体对外所做的功。(2)假如气体经绝热过程体积膨胀至原来的3倍,那么气体对外所做的功为多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“温度为25℃、压强为1.013x10^5Pa的1mol刚性双…”相关的问题
更多“温度为25℃、压强为1.013x10^5Pa的1mol刚性双…”相关的问题
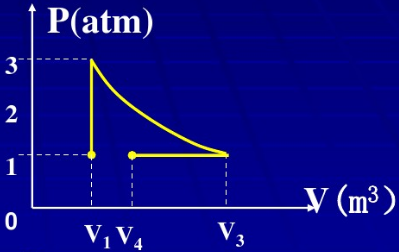
3mol温度为T0=273K的理想气体,先经等温过程体积膨胀到原来的5倍,然后等容加热,使其末态的压强刚好等于初始压强,整个过程传给气体的热量为8×104J.试画出此过程的p-V图,并求这种气体的摩尔热容比γ=Cp,m/CV,m值。
3mol的温度为T0=273K的理想气体,先经等温过程体积膨胀到原来的5倍,然后等体加热,使其末态的压强刚好等于初始压强,整个过程传给气体的热量为8×104J。试画出此过程的p-V图,并求出这种气体的比热容比γ=Cp/Cv值。[摩尔气体常量R=8.31J/(mol·K)]
1mol双原子分子理想气体在25℃、pθ分别经下列过程到体积增大一倍,求△S、△S环境和△S总。(1)恒温自由膨胀;(2)反抗外压为终态平衡压力(p外p2)恒温膨胀;(3)恒温可逆膨胀;(4)绝热自由膨胀;(5)绝热可逆膨胀。
一定量的双原子分子理想气体,其体积和压强按pV2=a的规律变化,其中a为已知常数。当气体从体积V1膨胀到V2。

如下图所示,质量为2.8g,温度为27℃,压强为1.013×105Pa的氮气,先经等压膨胀至体积加倍,再经等体过程至压强加倍,最后经等温过程,使其压强恢复至初态。试求气体在全过程中所做的功、吸收的热量和内能的改变量?
1mol刚性双原子分子理想气体,当温度为T时,其内能为()(式中R为摩尔气体常量,k为玻耳兹曼常量)。

2mol的理想气体,经历一可逆等温过程,体积从0.02m2膨胀到0.04m2,温度为300K。求其熵变为多少?
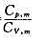 .
.
1mol氧气和1mol水蒸气(均视为刚性分子理想气体),若在体积不变的情况下吸收相等的热量,则它们的()。
A.温度升高相同,压强增加相同
B.温度升高不同,压强增加不同
C.温度升高相同,压强增加不同
D.温度升高不同,压强增加相同