 更多“理想气体的状态方程为()。”相关的问题
更多“理想气体的状态方程为()。”相关的问题
第1题
(1)某单原子理想气体的配分函数q具有的函数形式为q=Vf(T),试导出理想气体的状态方程;(2)若该
(1)某单原子理想气体的配分函数q具有的函数形式为q=Vf(T),试导出理想气体的状态方程;
(2)若该单原子理想气体的配分函数q的函数形式为q=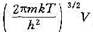 ,试导出压力P和热力学能U的表达式,以及理想气体的状态方程。
,试导出压力P和热力学能U的表达式,以及理想气体的状态方程。
第2题
理想气体的状态方程是pV=RT,若其中的压力p用逸度f代替后就成为真实气体的状态方程。 ()
理想气体的状态方程是pV=RT,若其中的压力p用逸度f代替后就成为真实气体的状态方程。 ( )
第3题
已知某理想气体的状态方程为PV=CT(C为恒量),则该气体的分子总数N=___________。(玻尔兹曼常量
已知某理想气体的状态方程为PV=CT(C为恒量),则该气体的分子总数N=___________。(玻尔兹曼常量为κ)
第4题
今有0℃,40530kPa的N2气体,分别用理想气体状态方程及范德华方程计算其摩尔体积。实验值为70.3cm3·mol-1。
今有0℃,40530kPa的N2气体,分别用理想气体状态方程及范德华方程计算其摩尔体积。实验值为70.3cm3·mol-1。
第5题
13. 今有0℃,40530kPa的N2气体,分别用理想气体状态方程及范德华方程计算其摩尔体积。实验值为70.3cm3·mol-1。
13. 今有0℃,40530kPa的N2气体,分别用理想气体状态方程及范德华方程计算其摩尔体积。实验值为70.3cm3·mol-1。


 如果结果不匹配,请
如果结果不匹配,请 
















