 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在含有0.2 mol.dm-3游离NH3的pH=10.0的氨性缓冲溶液中,以0.020 mol.dm-3EDTA滴定同浓度的Cu2+,计
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在含有0.2 mol.dm-3游离NH3的pH=10.0的氨…”相关的问题
更多“在含有0.2 mol.dm-3游离NH3的pH=10.0的氨…”相关的问题
在含有0.2mol·dm-3游离NH3的pH=10.0的氨性缓冲溶液中,以0.020mol·dm-3EDTA滴定同浓度的Cu2+,计算化学计量点时的pCu'。在上述相同条件下,如滴定的是0.020mol·dm-3Mg2+,化学计量点时的pMg是多少?若Cu2+与Mg2+同时存在,怎样才能进行连续滴定?简述其理由。(α(Cu(OH))=101.7,Cu2+-NH3络合物的lgβ1~lgβ4分别为4.31,7.98,11.02,13.82)
在pH=10.0、含有酒石酸盐(A)的氨性缓冲溶液中,以0.0200mol·L-1EDTA滴定同浓度的Cd2+,终点时游离氨的浓度为0.1mol·L-1。计算化学计量点时的pCd'sp和pCdsp各为多少?(lgKCdY=16.5,pH=10.0时,lgαY(H)=0.45,lgαCd(OH)=0.7,lgαCd(A)=3.8;Cd2+-NH3络合物的lgβ1-lgβ4分别为2.6、4.7、6.2、7.1。Cd2+与A形成1:1的络合物)
在pH=10的氨性缓冲溶液中,用EDTA滴定同浓度的Zn2+至化学计量点,下列关系式哪一个正确A)pZnsp=pZn‘ sp+lgαZn(NH3) B)pZnsp= pZn‘ sp -lgαZn(NH3) C)pZnsp=lgZn‘ sp+pαZn(NH3) D)pZnsp=lgαZn(NH3) - pZn‘ sp
A.滴定至化学计量点前,当滴定百分数相同时pZn'相等
B.化学计量点时pZn'目等
C.化学计量点后pZn'相等
D.化学计量点前、后及化学计量点时pZn'均不相等
 =0.5,
=0.5,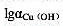 =0.8,PAN的
=0.8,PAN的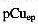 =13.8,Cu-NH3配合物的各级累积常数lgβ1~1gβ4:4.13,7.61,10.48,12.59。
=13.8,Cu-NH3配合物的各级累积常数lgβ1~1gβ4:4.13,7.61,10.48,12.59。
A.6.5
B.8.0
C.11.5
D.10.0
A.滴定开始时pZn相等
B.滴定至一半时pZn相等
C.滴定至化学计量点时,pZn相等
D.上述三种情况都不相等
以铬黑T(EBT)为指示剂,在pH=10的NH3-NH4Cl缓冲溶液中,用0.02000mol/LEDTA滴定0.02000mol/L的Zn2+时,存在共存离子Ag+,其浓度是0.010mol/L。若在化学计量点时游离NH3的浓度为0.10mol/L:(1)能否准确滴定Zn2+? (2)计算该滴定的误差。
[lgKZnY=16.50;lgKAgY=7.32;pH=10时,lgKZn-EBT=12.2,lgαEBT(H)=1.6,lgαY(H)=0.45;Zn2+和Ag+的水解作用可忽略;银氨配合物的lgβ1=3.40、lgβ2=7.40;锌氨配合物的lgβ1=2.27、lgβ2=4.61、lgβ3=7.01、lgβ4=9.06]
0.02 mol·L-1EDTA等浓度滴定Zn2+,在pH=10.0的NH4Cl-NH3介质中若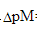 =0.2 mol·L-1,判断能否准确滴定。达化学计量点时,未络合的Zn2+百分数是多少?(pH=10.0时,αZn(OH)=102.4,lgαY(H)=0.5,lgKZnY=16.50,锌氨络合物的lgβ1~lgβ4分别为2.27、4.61、7.01、9.06
=0.2 mol·L-1,判断能否准确滴定。达化学计量点时,未络合的Zn2+百分数是多少?(pH=10.0时,αZn(OH)=102.4,lgαY(H)=0.5,lgKZnY=16.50,锌氨络合物的lgβ1~lgβ4分别为2.27、4.61、7.01、9.06