 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
利用附录C.2已知的数据,求下列电极反应的标准电极电势: (1)ClO3-+6H++6e=Cr-+3H2O (2)
利用附录C.2已知的
 数据,求下列电极反应的标准电极电势: (1)ClO3-+6H++6e=Cr-+3H2O (2)H2O2+2H++2e=2H2O
数据,求下列电极反应的标准电极电势: (1)ClO3-+6H++6e=Cr-+3H2O (2)H2O2+2H++2e=2H2O
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用附录C.2已知的
 数据,求下列电极反应的标准电极电势: (1)ClO3-+6H++6e=Cr-+3H2O (2)H2O2+2H++2e=2H2O
数据,求下列电极反应的标准电极电势: (1)ClO3-+6H++6e=Cr-+3H2O (2)H2O2+2H++2e=2H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“利用附录C.2已知的数据,求下列电极反应的标准电极电势: (…”相关的问题
更多“利用附录C.2已知的数据,求下列电极反应的标准电极电势: (…”相关的问题
已知电极反应:Cu++e-====Cu的

已知298.15K时,电极反应: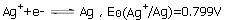 ,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e-
,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e- 2Ag+C2O2-4的标准电极电势
2Ag+C2O2-4的标准电极电势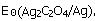 。
。
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g):
(1)利用附录(在教材中)中各物质的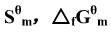 ,数据,求上述反应在25℃时的
,数据,求上述反应在25℃时的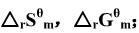
;(2)利用附录(在教材中)中各物质的△rGm数据,求上述反应在25℃时的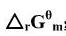 ;
;
(3)25℃时,若始态CH4(g)和CO2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的△rSm和△rGm。
已知25℃时,AgBr在纯水中的溶度积。Ag电极的标准电极电势,Br2(l)电极标准电极电势。试求25℃时:

已知电极反应 (Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应
(Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应 的标准电极电势
的标准电极电势
A.0.2576V
B.0.279V
C.1.081V
D.1.777V