 更多“同种金属及其盐溶液也能组成原电池,其条件是两个半电池中离子浓…”相关的问题
更多“同种金属及其盐溶液也能组成原电池,其条件是两个半电池中离子浓…”相关的问题
第3题
下列有关Cu-Zn原电池的叙述中,错误的是( )。
A.盐桥中的电解质可保持两个半电池中的电荷平衡
B.盐桥用于维持氧化还原反应的进行
C.盐桥中的电解质不能参与电池反应
D.电子通过盐桥流动
第4题
产生浓差极化的原因是()A.两个半电池中溶液浓度的不同B.电极附近和溶液内部电解质浓度的改变
产生浓差极化的原因是()
点击查看答案
A.两个半电池中溶液浓度的不同
B.电极附近和溶液内部电解质浓度的改变
C.电池的可逆性
D.测量时温度的变化
第5题
将锡和铅的金属片分别插入含有该金属离子的溶液中并组成原电、也(用图式表示,要注明浓度)。 (1)c(
将锡和铅的金属片分别插入含有该金属离子的溶液中并组成原电、也(用图式表示,要注明浓度)。 (1)c(Sn2+)=0.0100 mol.dm-3,c(Pb2+)=1.00 mol.dm-3; (2)c(Sn2+)=1.00 mol.dm-3,C(Pb2+)=0.100 mol.dm-3。 分别计算原电池的电动势,写出原电池的两电极反应和电池总反应式。
点击查看答案
第6题
在离子交换色谱法中,下列措施中能改变保留体积的是()。
A.改变离子的交换剂
B.以二价金属盐溶液代替一价金属盐溶液作流动相
C.降低流动相中盐的浓度
D.改变流速
E.改变流动相的pH
第7题
已知EΘ(Pb2+/Pb)=-0.126V,EΘ(Fe3+/Fe2+)=0.771V,(PbCl2)=1.6×10-5。在金属铅和硝酸铅溶液组成的半电池系统中
已知EΘ(Pb2+/Pb)=-0.126V,EΘ(Fe3+/Fe2+)=0.771V,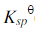 (PbCl2)=1.6×10-5。在金属铅和硝酸铅溶液组成的半电池系统中,加入NaCl(aq),沉淀完全后。当c(Cl-)=1.0mol·L-1时,该半电池的电极电势是多少?将该半电池与Fe3+/Fe2+标准半电池组成原电池。写出原电池符号及电池反应的离子方程式,并计算此原电池的标准电动势EΘ。
(PbCl2)=1.6×10-5。在金属铅和硝酸铅溶液组成的半电池系统中,加入NaCl(aq),沉淀完全后。当c(Cl-)=1.0mol·L-1时,该半电池的电极电势是多少?将该半电池与Fe3+/Fe2+标准半电池组成原电池。写出原电池符号及电池反应的离子方程式,并计算此原电池的标准电动势EΘ。
第8题
由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1)和Pt,H2(pΘ)丨H+(xmolL-1)组成一原电池,测得该原电池的
由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1)和Pt,H2(pΘ)丨H+(xmolL-1)组成一原电池,测得该原电池的电动势为0.016V,若pt,H2(pΘ)丨H+(xmolL-1)作为原电池的正极,问组成该半电池的溶液中H+浓度是多少?
点击查看答案


 如果结果不匹配,请
如果结果不匹配,请 
















