 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。
在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中超电势可忽略不计, (设活度因子均为1),试问:
(设活度因子均为1),试问:

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中超电势可忽略不计, (设活度因子均为1),试问:
(设活度因子均为1),试问:

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解…”相关的问题
更多“在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解…”相关的问题
在298K和标准压力下,用铁Fe(s)为阴极,C(石墨)为阳极,电解6.0mol·kg-1的NaCl水溶液。若H2(g)在铁阴极上的超电势为0.20V,O2(g)在石墨阳极上的超电势为0.60V,Cl2(g)的超电势可忽略不计,试说明两极上首先发生的反应及计算至少需加多少外加电压,电解才能进行(设活度因子均为1)。
298K、 下,以Pt为阴极,电解含FeCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中不断搅拌,超电势可略去不计,并设活度因子均11。试问:
下,以Pt为阴极,电解含FeCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中不断搅拌,超电势可略去不计,并设活度因子均11。试问:
(1) 何种金属先析出?
(2) 第二种金属析出时至少需施加多大电压?
298K时,以Pt为阳极,Fe为阴极,电解浓度为1mol·kg-1的NaCl水溶液(活度因子为0.66)。设电极表面有H2(g)不断逸出时的电流密度为0.1A·cm-2,Pt逸出Cl2(g)的超电势可近似视为零。若Tafel公式为 ,且Tafel常数a=0.73V,b=0.11V,
,且Tafel常数a=0.73V,b=0.11V,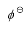 =1.36V,请计算实际的分解电压。
=1.36V,请计算实际的分解电压。
在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混合溶液。已知Cd2+和Zn2+的浓度均为0.10mol·kg-1(设活度因子均为1),H2(g)在Cd(s)和Zn(s)上的超电势分别为0.48V和0.70V,设电解液的pH值保持为7.0。试问:

在298K时使下述电解池发生电解作用:
Pt(s)|CdCl2(1.0mol·kg-1),NiSO4(1.0mol·kg-1)|Pt(s)
问当外加电压逐渐增加时,两电极上首先分别发生什么反应?这时外加电压至少为多少?(设活度因子均为1,超电势可忽略。)
在298K和标准压力下,某混合溶液中,CuSO4浓度为0.50mol·kg-1,H2SO4浓度为0.01mol·kg-1,用铂电极进行电解,首先Cu(s)沉积到Pt电极上。若H2(g)在Cu(s)上的超电势为0.23V,问当外加电压增加到有H2(g)在电极上析出时,溶液中所余Cu2+的浓度为多少?(设活度因子均为1,H2SO4作一级解离处理。)
在298K和标准压力下,当电流密度为0.1A·cm-2时,H2(g)和O2(g)在Ag(s)电极上的超电势分别为0.87V和0.98V。今用Ag(s)电极电解浓度为0.01mol·kg-1的NaOH溶液,问这时在两个银电极上首先发生什么反应?此时外加电压为多少(设活度因子为1)?