 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
相对密度为1.01的含3.00%的H2O2溶液2.50mL,与的KMnO4溶液完全作用,需此浓度的KMn
相对密度为1.01的含3.00%的H2O2溶液2.50mL,与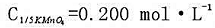 的KMnO4溶液完全作用,需此浓度的KMnO4溶液多少毫升?已知滴定反应为
的KMnO4溶液完全作用,需此浓度的KMnO4溶液多少毫升?已知滴定反应为
5H2O2+2MnO4-+6H+=2Mn2++5O2+8H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
相对密度为1.01的含3.00%的H2O2溶液2.50mL,与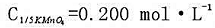 的KMnO4溶液完全作用,需此浓度的KMnO4溶液多少毫升?已知滴定反应为
的KMnO4溶液完全作用,需此浓度的KMnO4溶液多少毫升?已知滴定反应为
5H2O2+2MnO4-+6H+=2Mn2++5O2+8H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“相对密度为1.01的含3.00%的H2O2溶液2.50mL,…”相关的问题
更多“相对密度为1.01的含3.00%的H2O2溶液2.50mL,…”相关的问题
A、酸式滴定管用蒸馏水洗净后,直接加入已知浓度的KMnO4溶液
B、锥形瓶用蒸馏水洗净后,直接移取一定体积的未知浓度的H2O2溶液
C、滴定时,不用排出滴定管下口的气泡
D、滴定时需加入其他指示剂
已知某KMnO4溶液在酸性溶液中对Fe2+的滴定度为0.005585g/mL,而20.00mL上述KMnO4溶液在酸性介质中恰好与10.00mL H2C2O4溶液完全反应,求等量的H2C2O4与0.1000mol/L NaOH溶液反应时,需要NaOH溶液的毫升数。
已知在酸性溶液中,Fe2+与KMnO4反应时,1.00mL KMnO4溶液相当于0.1117g Fe,而1.00mL KHC2O4·H2C2O4溶液在酸性介质中恰好与0.20mL上述KMnO4溶液完全反应。问需要多少毫升0.2000mol/L NaOH溶液才能与上述1.00mL KHC2O4·H2C2O4溶液完全中和?(已知MFe=55.85)
已知在酸性溶液中,Fe2+与KMnO4反应时,1.00mLKMnO4溶液相当于0.1117gFe,而1.00mLKHC2O4·H2C2O4溶液在酸性介质中恰好与0.20mL上述KMnO4溶液完全反应。问需要多少毫升0.2000mol·L-1NaOH溶液才能与上述1.00mLKHC2O4·H2C2O4溶液完全中和?
标定KMnO4溶液的浓度时,称取草酸钠0.2262g,用水溶解后,在适当条件下,用KMnO4溶液滴定,消耗KMnO4溶液41.50mL。计算此KMnO4溶液的浓度及对Fe的滴定度。已知M(Na2C2O4)=134.0g·mol-1,M(Fe)=55.85g·mol-1。