 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知甲醇蒸气的标准生成吉布斯自由能为-161.96kJ/mol。试求甲醇(液)的标准生成自由能(假定气体为理想气体,且
已知甲醇蒸气的标准生成吉布斯自由能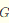 为-161.96kJ/mol。试求甲醇(液)的标准生成自由能(假定气体为理想气体,且已知298.15K的蒸气压为16.59kPa)。
为-161.96kJ/mol。试求甲醇(液)的标准生成自由能(假定气体为理想气体,且已知298.15K的蒸气压为16.59kPa)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知甲醇蒸气的标准生成吉布斯自由能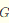 为-161.96kJ/mol。试求甲醇(液)的标准生成自由能(假定气体为理想气体,且已知298.15K的蒸气压为16.59kPa)。
为-161.96kJ/mol。试求甲醇(液)的标准生成自由能(假定气体为理想气体,且已知298.15K的蒸气压为16.59kPa)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知甲醇蒸气的标准生成吉布斯自由能为-161.96kJ/mo…”相关的问题
更多“已知甲醇蒸气的标准生成吉布斯自由能为-161.96kJ/mo…”相关的问题
298K时. 已知甲醇蒸气的标准摩尔Gibbs生成自由能为-161.92kJ·mol-1,试求甲醇液体的标准摩尔Gibbs生成自由能。已知该温度下甲醇液体的饱和蒸气压为16.343kPa。假定气体为理想气体。
已知25℃时液态水的标准摩尔生成吉布斯函数为-237.129kJ·mol-1·K-1,水在25℃时的饱和蒸气压ps=3.1663kPa。求25℃时水蒸气的标准摩尔生成吉布斯函数。
已知25℃时液态水的标准摩尔生成吉布斯函数为-237.129kJ·mol-1,水在25℃时的饱和蒸气压pθ=3.1663kPa。求25℃时水蒸气的标准摩尔生成吉布斯函数。
已知298.15K,CO(g)和CH3OH(g)标准摩尔生成焓ΔfHm分别为-110.525kJ/mol和-200.67kJ/mol;CO(g)、H2(g)、CH3OH(l)的标准摩尔熵 分别为197.674,130.684及126.8J/(mol·K)。又知298.15K甲醇的饱和蒸气压为16.59kPa,摩尔气化热
分别为197.674,130.684及126.8J/(mol·K)。又知298.15K甲醇的饱和蒸气压为16.59kPa,摩尔气化热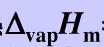 =38.0kJ/mol,蒸气可视为理想气体。
=38.0kJ/mol,蒸气可视为理想气体。
利用上述数据,求298.15K时,反应CO(g)+2H2(g)====CH3OH(g)的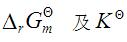 .
.
.66kPa,在蒸气中A的摩尔分数为0.60。假定蒸气为理想气体,试求:(1)溶液中A和B的活度;(2)溶液中A和B的活度系数;(3)混合过程的Gibbs自由能变化值△mixGre;(4)如果溶液是理想的,求混合过程的Gibbs自由能变化值△mixGid。
已知298.15K时,CO(g)和CH3OH(g)标准摩尔生成焓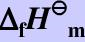 分别为-110.525和-200.66kJ/mol。CO(g)、H2(g)、CH3OH(l)的标准摩尔熵
分别为-110.525和-200.66kJ/mol。CO(g)、H2(g)、CH3OH(l)的标准摩尔熵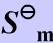 (298.15K)分别为197.67J/(mol·K)、130.68J/(mol·K)及127J/(mol·K)。又知298.15K时甲醇的饱和蒸气压16.59kPa,摩尔气化热
(298.15K)分别为197.67J/(mol·K)、130.68J/(mol·K)及127J/(mol·K)。又知298.15K时甲醇的饱和蒸气压16.59kPa,摩尔气化热 =38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应
=38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应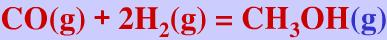 的
的