 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
一化学反应系统在等温定容条件下发生一变化,可通过两个不同途径完成:(1)放热10kJ,做电功50kJ;(2)放热Q,不做功。则:
A.Q=-10kJ;
B.Q=-60kJ;
C.Q=-40kJ;
D.此反应的QV=-10kJ。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Q=-10kJ;
B.Q=-60kJ;
C.Q=-40kJ;
D.此反应的QV=-10kJ。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一化学反应系统在等温定容条件下发生一变化,可通过两个不同途径…”相关的问题
更多“一化学反应系统在等温定容条件下发生一变化,可通过两个不同途径…”相关的问题
化学反应A(g)+B(g)====2C(g),A、B、C均为理想气体。在298K,标准状态下,该过程分别按下列两个途径完成:(1) 不作功,放热41.8kJ;(2) 作最大功,放热1.64kJ。则在(1)、(2)两种情况下,变化过程的Q、W、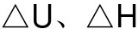 各是多少?
各是多少?
A.不作非体积功条件下,QV与途径无关,故QV是状态函数;
B.不作非体积功条件下,Qp与途径无关,故Qp是状态函数;
C.系统发生一确定变化,不同途径中,热肯定不相等;
D.系统发生一确定变化,则Q+W与途径无关。
A.1300J
B.300J
C.-300J
D.700J