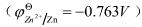题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
若在标准氢电极中加入NaAc溶液,当ρ(H2)=100kPa,c(HAc)=c(Ac-)=1.0mol·L-1时,求ψ(H+/H2)的值。
若在标准氢电极中加入NaAc溶液,当ρ(H2)=100kPa,c(HAc)=c(Ac-)=1.0mol·L-1时,求ψ(H+/H2)的值。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若在标准氢电极中加入NaAc溶液,当ρ(H2)=100kPa,c(HAc)=c(Ac-)=1.0mol·L-1时,求ψ(H+/H2)的值。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若在标准氢电极中加入NaAc溶液,当ρ(H2)=100kPa…”相关的问题
更多“若在标准氢电极中加入NaAc溶液,当ρ(H2)=100kPa…”相关的问题
已知标准氢电极的电极反应为2H+ + 2e = H2(g)求算在0.10mol·L-1的HAc溶液中、氢气的压力为100 kPa时,氢电极的电势。
玻璃电极|标准溶液或未知液||饱和甘汞电极
当标准缓冲溶液的pH=4.00时电动势为0.209V,当缓冲溶液由未知溶液代替时,测得下到电动势值:①0.088V;②0.312V。求未知溶液的pH值。
A.氢电极的电极电势为0V;
B.标准氢电极的电极电势为0V;
C.298.15K时,氢电极的标准电极电势为0V;
D.标准氢电极中,Pt与溶液之间的电势差为0V。
(-)玻璃电极|标准溶液或未知液||饱和甘汞电极()当标准缓冲溶液的pH=4.00时电动势为0.209V,当缓冲溶液由未知溶液代替时,测得下列电动势值(1) 0.088V;(2) 0.312V。求未知溶液的pH值。
若氢电极为一缓冲溶液时,测得电池电动势为0.427V,求缓冲溶液的pH。
电池反应: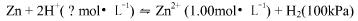 ,其中c(Zn2+)=1.00mol·L-1,P(H2)=100kPa,298.15K时测其电池的电动势为+0.460V,求氢电极溶液中的pH值是多少?
,其中c(Zn2+)=1.00mol·L-1,P(H2)=100kPa,298.15K时测其电池的电动势为+0.460V,求氢电极溶液中的pH值是多少?