 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将某一元弱酸HA溶于未知量水中,并用一未知浓度的强碱去滴定:当用去3.05 cm3强碱时,溶液pH=4.00;
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将某一元弱酸HA溶于未知量水中,并用一未知浓度的强碱去滴定:…”相关的问题
更多“将某一元弱酸HA溶于未知量水中,并用一未知浓度的强碱去滴定:…”相关的问题
将一未知一元弱酸溶于未知量水中,用浓度为0.1000mol·dm-3的某一元强碱去滴定。已知当用去10.00mL强碱时,溶液的pH=4.50;当用去24.60mL强碱时,滴定至终点。问该弱酸的解离常数是多少?
称取不纯的未知弱酸HA试样1.600g,溶于60.00mL水中,用0.2500mol·L-1NaOH溶液滴定。已知中和HA至50%时,溶液的pH=5.00,当中和至化学计量点时,pH=9.00。计算试样中HA的百分含量为多少。(设HA的摩尔质量为82.00g·mol-1)
称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示剂,用0.1000mol/LNaOH滴定,当滴定剂加到10.50mL时,溶液的pH为4.20;滴定至终点时,消耗NaOH溶液24.70mL。求:

称取一元弱酸HA试样1.000g,溶于60.0mL水中,用0.2500mol·L-1。NaOH溶液滴定。已知中和HA至50%时,溶液的pH=5.00;当滴定至化学计量点时,pH=9.00。计算试样中HA的质量分数。(假设HA的摩尔质量为82.00g·mol-1。)
A.强碱滴定强酸
B.强碱滴定弱酸
C.强酸滴定强碱
D.强酸滴定混合弱碱或多元碱
用NaOH溶液滴定某弱酸HA时(两者浓度相同),当滴定至一半时,溶液的pH值为5.00;当滴定至化学计量点时,溶液的pH值为8.00;当滴定至200%时溶液pH值为12.00。则该酸(HA)的pKa值是()。
A.5.00
B.8.00
C.12.00
D.7.00
滴定突跃范围一定在偏碱性区的是
(A) 强酸滴定强碱 (B) 强酸滴定一元弱碱
(C) 强碱滴定一元弱酸 (D) 强碱滴定多元强酸
一元弱酸能被强碱直接准确滴定的条件是cKa≥__________,多元酸能被强碱分步滴定的条件是 Ka1/Ka2≥__________,混合酸HA,HB其浓度分别为c1,c2,若它们的cKa足够大,则能被强碱分步滴定的条件是
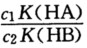 __________,H3BO3的Ka=6.4×10-10,应加_________试剂,使弱酸强化,能用NaOH滴定。
__________,H3BO3的Ka=6.4×10-10,应加_________试剂,使弱酸强化,能用NaOH滴定。