 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某溶液中含有1.00 mol·kg-1的Zn(NO3)2和1.00 mol·kg-1的Cu(NO3)2,pH=4.0,该溶液在25℃时,用
某溶液中含有1.00 mol·kg-1的Zn(NO3)2和1.00 mol·kg-1的Cu(NO3)2,pH=4.0,该溶液在25℃时,用光滑的Pt片作为电极。试问当阴极电势达-0. 30 V时,阴极上发生什么反应?这时溶液中残余Cu2+的浓度为多少?已知H2在光滑Pt片和Cu片上的超电势分别为0.1V和0.2v,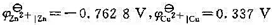 .假设不考虑其活度因子的影响。
.假设不考虑其活度因子的影响。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“某溶液中含有1.00 mol·kg-1的Zn(NO3)2和1…”相关的问题
更多“某溶液中含有1.00 mol·kg-1的Zn(NO3)2和1…”相关的问题
1.jpg) 假设电解过程中保持溶液的pH=7,析出的H2(g)压力为100kPa。
假设电解过程中保持溶液的pH=7,析出的H2(g)压力为100kPa。1.jpg)
















