题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
可逆反应在密闭容器中建立平衡,在749K时该反应的平衡常数Kc=2.6。 (1)求n(H2O)/n(CO)(物质的量比)为1时,CO
可逆反应CO+H2O CO2+H2在密闭容器中建立平衡,在749K时该反应的平衡常数Kc=2.6。
(1)当CO 起始浓度为2mol/L,H2O 起始浓度为2mol/L 时,CO 的转化率为多少?(2)当CO 起始浓度仍为2mol/L,H2O 的起始浓度为6mol/L 时,CO 的转化率为多少?
(3)从计算结果说明浓度对化学平衡移动的影响。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“可逆反应在密闭容器中建立平衡,在749K时该反应的平衡常数K…”相关的问题
更多“可逆反应在密闭容器中建立平衡,在749K时该反应的平衡常数K…”相关的问题
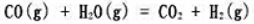 在749K时的平衡常数K0=2.6。设(1)反应起始时CO和H2O的浓度都为1mol/L(没有生产物,下同);(2)起始时CO和H2O的摩尔比为1比3,求CO的平衡转化率。用计算结果来说明勒夏特列原理。
在749K时的平衡常数K0=2.6。设(1)反应起始时CO和H2O的浓度都为1mol/L(没有生产物,下同);(2)起始时CO和H2O的摩尔比为1比3,求CO的平衡转化率。用计算结果来说明勒夏特列原理。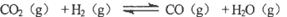 其平衡常数K和温度,的关系如下:
其平衡常数K和温度,的关系如下: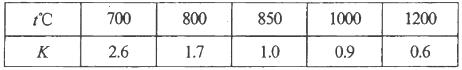
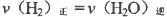 B.混合气体中CO浓度不变
B.混合气体中CO浓度不变

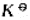 =2.6,试计算:
=2.6,试计算: 在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
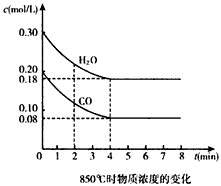
 CO2(g)+ H2(g) △H<0。CO和H2O浓度变化如图:
CO2(g)+ H2(g) △H<0。CO和H2O浓度变化如图: