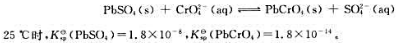题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,酸催化蔗糖转化反应: C12H22O11(蔗糖)+H2O→C6H12O6(葡萄糖)+C6H12O6(果糖) 的动力学数据如表11-2
25℃时,酸催化蔗糖转化反应:
C12H22O11(蔗糖)+H2O→C6H12O6(葡萄糖)+C6H12O6(果糖)
的动力学数据如表11-2所示(蔗糖初始浓度c0=1.0023mol·dm-3,时刻t的浓度为ctd)。试用作图法证明此反应为一级反应。求算速率常数及半衰期;问蔗糖转化95%需时多少?
表11-2 | ||||||
t/min | 0 | 30 | 60 | 90 | 130 | 180 |
(c0-c)/(mol·dm-3) | 0 | 0.1001 | 0.1946 | 0.2770 | 0.3726 | 0.4676 |
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“25℃时,酸催化蔗糖转化反应: C12H22O11(蔗糖)+…”相关的问题
更多“25℃时,酸催化蔗糖转化反应: C12H22O11(蔗糖)+…”相关的问题
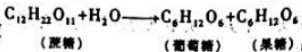 的动力学数据如下(蔗糖的初始浓度co为1.0023mol●dm-3,时刻t,时的浓度为c):
的动力学数据如下(蔗糖的初始浓度co为1.0023mol●dm-3,时刻t,时的浓度为c):
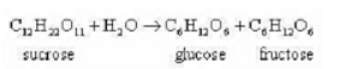 的动力学数据如下(蔗糖的初始浓度c为1.0023mol·dm-3,时刻t的浓度为c)
的动力学数据如下(蔗糖的初始浓度c为1.0023mol·dm-3,时刻t的浓度为c)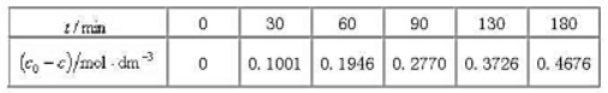
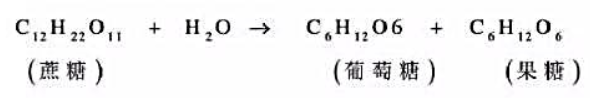

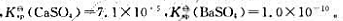 则沉淀转化反应:
则沉淀转化反应: 在25℃时的标准平衡常数
在25℃时的标准平衡常数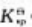 =()。在25℃标准状态下,上述反应方向为()。
=()。在25℃标准状态下,上述反应方向为()。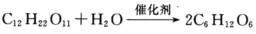 是一级反应。在25℃速率常数为5.7×10-5s-1。问: (1)浓度为1mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
是一级反应。在25℃速率常数为5.7×10-5s-1。问: (1)浓度为1mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。