 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知在967 K时,反应的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
已知在967 K时,反应
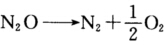 的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在967 K时,反应
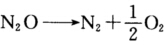 的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知在967 K时,反应的速率常数k=0.1 35 s-1,…”相关的问题
更多“已知在967 K时,反应的速率常数k=0.1 35 s-1,…”相关的问题
已知某气相反应的活化能Ea=163kJ·mol-1,温度390K时的速率常数k=2.37×10-2dm3·mol-1·s-1。试求温度为420K时的反应速率常数。
已知某反应288K时,速率常数为3.1×10-3,而313K时速率常数为1.5×10-2,求该反应的活化能。
已知反应HI(g)+CH3I(g)→CH4(g)+I2(g)在157℃时的速率常数k=l.7×10-5L·mol-1·s-1,在227℃时的速率常数k=4.0×10-3L·mol-1·s-1,求该反应的活化能。
已知液态松节油萜的消旋作用是一级反应,在458K和510K时速率常数分别为k(458K)=2.2×10-5min-1和k(510K)=3.07×10-3min-1。试求反应的实验活化能Ea,以及在平均温度时的活化焓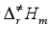 、活化熵
、活化熵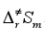 和活化Gibbs自由能
和活化Gibbs自由能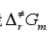 。
。
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.mol-1,分子的碰撞直径为3.50×10-10m。试确定反应速率常数kHI与温度的关系式并求556K时的反应速率常数。
反应2HI→H2+I2在无催化剂存在时,其活化能Ea(非催化)一184.1kJ·mol-1,在以Au作催化剂时,反应的活化能Ea(催化)=104.8kJ·mol-1,若反应在503K时进行,如果指前因子A(催化)值比A(非催化)值小1×103倍,试估计以Au为催化剂的反应速率常数将比非催化的反应速率常数大多少倍?