 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知水的离子积常数 在293 K和303K时分别为 和 .试求:(1) 298 K和标准压力时,中和反应 (1)的
已知水的离子积常数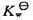 在293 K和303K时分别为
在293 K和303K时分别为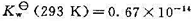 和
和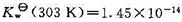 .试求:(1) 298 K和标准压力时,中和反应
.试求:(1) 298 K和标准压力时,中和反应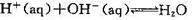 (1)的
(1)的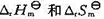 的值(设
的值(设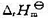 与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能
与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能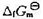 的值。
的值。
已知下述电池的标准电动势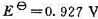 :
:
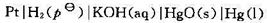
并已知反应 .
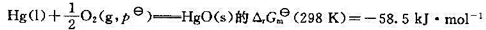
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知水的离子积常数 在293 K和303K时分别为 和 .试…”相关的问题
更多“已知水的离子积常数 在293 K和303K时分别为 和 .试…”相关的问题
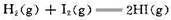

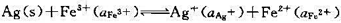 的平衡常数;
的平衡常数;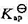 。
。 =-285.83kJ·mol-1,试求:该电池的温度系数
=-285.83kJ·mol-1,试求:该电池的温度系数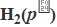 |Pt
|Pt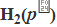


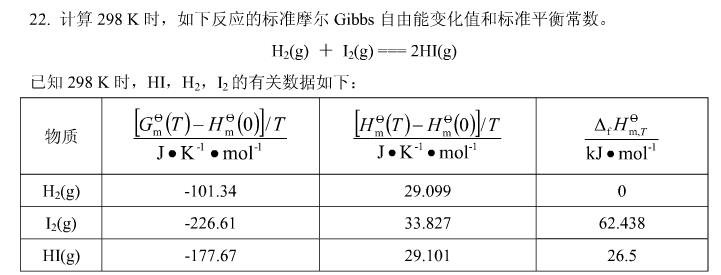
 CO2(g)在该温度时反应的标准Gibbs自由能
CO2(g)在该温度时反应的标准Gibbs自由能















