 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法中,正确的是 ()A.相同原子间的双键键能是单键键能的两倍B.原子形成共价键的数目
下列说法中,正确的是 ()
A.相同原子间的双键键能是单键键能的两倍
B.原子形成共价键的数目等于基态原子的未成对电子数
C.分子轨道是由同一原子中能量相近、对称性匹配的原子轨道组合而成
D.py和dxy的线性组合形成π成键轨道和π*反键轨道
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法中,正确的是 ()
A.相同原子间的双键键能是单键键能的两倍
B.原子形成共价键的数目等于基态原子的未成对电子数
C.分子轨道是由同一原子中能量相近、对称性匹配的原子轨道组合而成
D.py和dxy的线性组合形成π成键轨道和π*反键轨道
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列说法中,正确的是 ()A.相同原子间的双键键能是单键键能…”相关的问题
更多“下列说法中,正确的是 ()A.相同原子间的双键键能是单键键能…”相关的问题
下列说法中,正确的是( )
A.相同原子间的双键键能是单键键能的两倍
B.原子形成共价键的数目等于基态原子的未成对电子数
C.分子轨道是由同一原子中能量相近、对称性匹配的原子轨道组合而成
D.py和dxy的线性组合形成π成键轨道和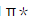 反键轨道
反键轨道
A.同原子间双键键能是单键键能的两倍
B.原子形成共价键的数目,等于基态原子的未成对电子数
C.分子轨道是同一个原子中的能量相近似、对称匹配的原子轨道线性组合而成
D.py和py的线性组合形成π键轨道和π*反键轨道
下列说法中正确的是
(A) 相同原子间双键键能是单键键能的两倍
(B) 原子形成共价键的数目,等于基态原子未成对电子数
(C) 分子轨道是由同一原子中能量近似,对称性匹配的原子轨道线性组合而成
(D) N2是反磁性的,而 是顺磁性的
是顺磁性的
(A) 元素原子在化合物中形成共价键的数目等于该基态原子未成对的电子数;
(B) 同核双原子分子双键的键能等于其单键键能的两倍;
(C) 分子内氢键的形成将使该物质的熔点和沸点降低;
(D) 分子的极性只与键的极性有关。
(A) 所有原子轨道都参与杂化
(B) 同一原子中能量相近的原子轨道参与杂化
(C) 杂化轨道能量集中,有利于牢固成键
(D) 空轨道也能进行杂化