 更多“某反应的活化能为117.15 kJ.mol-1,试计算在什么…”相关的问题
更多“某反应的活化能为117.15 kJ.mol-1,试计算在什么…”相关的问题
第1题
某反应的活化能为117.15kJ·mol-1,试计算在什么温度下反应速率是400K时反应速率的2倍?
某反应的活化能为117.15kJ·mol-1,试计算在什么温度下反应速率是400K时反应速率的2倍?
第2题
如果一反应的活化能为117.5kJ·mol-1,试问在什么温度时反应的速率常 数k的值是400K时速率常数的2倍。
如果一反应的活化能为117.5kJ·mol-1,试问在什么温度时反应的速率常 数k的值是400K时速率常数的2倍。
第3题
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算(1)400K时,反应
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
第4题
若某反应的活化能为80kJ·mol-1,则反应温度由20℃增加到30℃,其反应速率常数约为原来的 (A) 2倍 (B) 3倍 (
若某反应的活化能为80kJ·mol-1,则反应温度由20℃增加到30℃,其反应速率常数约为原来的
(A) 2倍 (B) 3倍 (C) 4倍 (D) 5倍
第5题
反应2NOCl(g)→2NO(g)+Cl2(g)的活化能为101kJ·mol-1,300K时,速率常数k1为2.80×10-5dm3·mol-1·s-1,试求400K时
反应2NOCl(g)→2NO(g)+Cl2(g)的活化能为101kJ·mol-1,300K时,速率常数k1为2.80×10-5dm3·mol-1·s-1,试求400K时的速率常数k2。
第6题
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率常数。
第7题
反应,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催
反应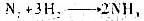 ,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
第9题
某反应的活化能为80kJ.mol—1,当反应温度由293K增加到303K时,其反应速率增加为原来的5倍。()
某反应的活化能为80kJ.mol—1,当反应温度由293K增加到303K时,其反应速率增加为原来的5倍。()
此题为判断题(对,错)。
第10题
某反应在温度由20℃升至30℃时,反应速率恰好增加1倍,则该反应的活化能为______kJ·mol-1。
某反应在温度由20℃升至30℃时,反应速率恰好增加1倍,则该反应的活化能为______kJ·mol-1。


 如果结果不匹配,请
如果结果不匹配,请 
















