 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列反应的(1)(298.15K);(2)(298.15K);(3)298.15K进行1mol反应时的体积功w。
计算下列反应的(1)


 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列反应的(1)


 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算下列反应的(1)(298.15K);(2)(298.15…”相关的问题
更多“计算下列反应的(1)(298.15K);(2)(298.15…”相关的问题
计算下列反应的(1)△rHΘm(298.15 K);(2)△rHΘm(298.15 K);(3)298.15 K进行1mol反应时的体积功W。 CH4(g)+4Cl2(g)=CCl4(l)+4HCl(g)
计算下列反应的平衡常数,判断反应进行的方向,并作简要说明(设参加反应各物质的浓度为1mol·L-1)。
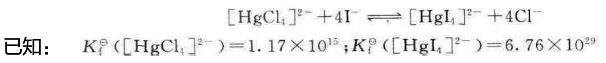
8.在298.15K时,有下列反应
H3AsO4+2I-+2H+====H3AsO3+I2+H2O
(1) 计算该反应组成的原电池的标准电动势。
(2) 计算该反应的标准摩尔吉布斯自由能变并指出该反应能否自发进行。
(3) 若溶液的的pH=7,而c(H3AsO4)=c(H3AsO3)=c(I-)=1mol·dm-3此反应的△rGm是多少?此时反应进行方向?
根据下列反应组成电池
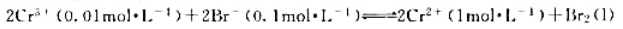
(1)写出电池符号;
(2)计算298K时的电动势,并判断反应自发进行的方向;
已知
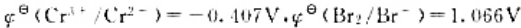
计算下列电池各电极的电极电势和电池电动势,并写出电池反应方程式:
(1)(—)Pt|H2(100kPa)|H+(2.0mol·L-1)||Cl-(1mol·L-1)|AgCl|Ag()
(2)(—)Pt|Sn2+(0.1mol·L-1),Sn4+(1mol·L-1)||Cl-(0.1mol·L-1)|Cl2(100kPa)|Pt()
(3)(—)Cu|Cu2+(0.1mol·L-1)||Cu2+(1.0mol·L-1)l Cu()
计算下列转化反应的平衡常数,并判断转化反应能否进行?
(1)[Cu(NH3)2]++2CN-===[Cu(CN)2]-+2NH3
(2)[Cu(NH3)4]2++Zn2+===[Zn(NH3)4]2++Cu2+
(3)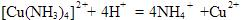
(4)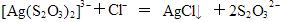
计算下列电池各电极的电极电势和电池电动势,并写出电池反应方程式:
(—)Pt|H2(100kPa)|H+(2.0mol·L-1)||Cl-(1mol·L-1)|AgCl|Ag()
制备半导体材料时发生如下反应,并已知相应热力学数据:
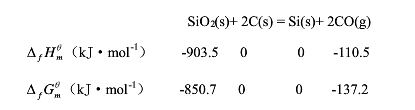
通过计算回答下列问题:
(1)标态下,398.15K时,反应能否自发进行
(2)标态下,反应自发进行的温度