 更多“求插入纯水的氢电极与标准氢电极所组成的原电池的电动势。”相关的问题
更多“求插入纯水的氢电极与标准氢电极所组成的原电池的电动势。”相关的问题
第1题
当P(H2)=100kPa和纯水构成氢电极与标准氢电极组成原电池时,其电动势E为 (A) 0.4144V (B) -0.4144V (C)
当P(H2)=100kPa和纯水构成氢电极与标准氢电极组成原电池时,其电动势E为
点击查看答案
(A) 0.4144V (B) -0.4144V (C) 0V (D) 0.8288V
第2题
将标准氢电极与另一氢电极组成原电池,若使电池的电动势最大,另一氢电极所采用的酸性溶液应是 (A) 0.1mol·
将标准氢电极与另一氢电极组成原电池,若使电池的电动势最大,另一氢电极所采用的酸性溶液应是
点击查看答案
(A) 0.1mol·dm-3HCl; (B) 0.1mol·dm-3HAc+0.1mol·dm-3NaAC;
(C) 0.1mol·dm-3HAc; (D) 0.1mol·dm-3H2SO4。
第4题
由标准氢电极和镍电极组成原电池。若c(Ni2+)=0.010mol·dm-3时,电池的电动势为0.2955V,其中镍为负极,计算镍电
由标准氢电极和镍电极组成原电池。若c(Ni2+)=0.010mol·dm-3时,电池的电动势为0.316V,其中镍为负极,计算镍电极的标准电极电势。
第5题
由镍电极和标准氢电极组成原电池,若c(Ni2+)=0.0100mol·dm-3时,原电池的电动势为0.315V,其中镍为负极,计算镍
由镍电极和标准氢电极组成原电池,若c(Ni2+)=0.0100mol·dm-3时,原电池的电动势为0.315V,其中镍为负极,计算镍电极的标准电极电势。
第6题
当以镍电极做负极和标准氢电极组成原电池,c(Ni2+)=0.0100mol·dm-3时,测得此原电池电动势E=0.316 V,则镍电极
当以镍电极做负极和标准氢电极组成原电池,c(Ni2+)=0.0100mol·dm-3时,测得此原电池电动势E=0.316 V,则镍电极的标准电极电势为______。
点击查看答案
第7题
某氢电极[p(H2)=100kPa]所用的溶液由浓度均为1.0mol·L-1的弱酸HA和其钠盐NaA组成。若将此氢电极与另一电极组成原电池,测得原电池的电动势E=0.38V,并知该氢电极为正极,另一电极的电极电势为E-=-0.65V.试计算该氢电极中溶液的pH和弱酸HA的标准解离常数。
第8题
6.由标准氢电极和镍电极组成原电池。若c(Ni2+)=0.010mol·dm-3时,电池的电动势为0.309V,其中镍为负极,计算镍
6.由标准氢电极和镍电极组成原电池。若c(Ni2+)=0.010mol·dm-3时,电池的电动势为0.309V,其中镍为负极,计算镍电极的标准电极电势。
第9题
将铜片插入含1.0mol·L-1氨水和1.0mol·L-1[Cu(NH3)4]2+的溶液中构成一个半电池,将此半电池与标准氢电极组成
将铜片插入含1.0mol·L-1氨水和1.0mol·L-1[Cu(NH3)4]2+的溶液中构成一个半电池,将此半电池与标准氢电极组成原电池,测得其电动势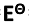 =0.030V,且知标准氢电极在此作正极。试计算[Cu(NH3)4]2+的K稳。(已知:
=0.030V,且知标准氢电极在此作正极。试计算[Cu(NH3)4]2+的K稳。(已知: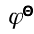 (Cu2+/Cu)=0.337V)
(Cu2+/Cu)=0.337V)


 如果结果不匹配,请
如果结果不匹配,请 
















