 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
0.02mol·dm-3EDTA等浓度滴定Zn2+,在pH=10的NH4Cl-NH3缓冲溶液中,,判断能否准确滴定?达到终点时未配合的Zn2+
0.02mol·dm-3EDTA等浓度滴定Zn2+,在pH=10的NH4Cl-NH3缓冲溶液中,

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
0.02mol·dm-3EDTA等浓度滴定Zn2+,在pH=10的NH4Cl-NH3缓冲溶液中,

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“0.02mol·dm-3EDTA等浓度滴定Zn2+,在pH=…”相关的问题
更多“0.02mol·dm-3EDTA等浓度滴定Zn2+,在pH=…”相关的问题
在pH=9.0的缓冲溶液中,加入某金属指示剂,用0.020mol/LEDTA滴定同浓度的Ni2+、Cd2+混合液中的Cd2+,请问:
(1)不加入掩蔽剂时,能否准确滴定?(以ITEI≤0.1%判断)
(2)加入掩蔽剂KCN,终点时游离的掩蔽剂总浓度为2.7x10^-6mol/L,判断能否准确滴定并计算滴定的终点误差。
(已知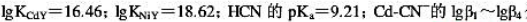 分别为5.48、10.60、15.23、18.78;Ni-CN-的lgβ4=31.3;pH=9.0时,
分别为5.48、10.60、15.23、18.78;Ni-CN-的lgβ4=31.3;pH=9.0时,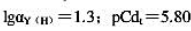 )
)
A.两种情况下浓度相等
B.前者大于后者
C.后者大于前者
D.无法判断
E.以上都不正确
用浓度为cEDTA=0.0500mol·dm-3的溶液滴定100.0cm3浓度为
实验证明,以铬黑T(EBT)为指示剂,于pH=9.6的氨性缓冲溶液中,用2.0×10-2mol·dm-3EDTA滴定同浓度的Mg2+时,准确度很高。试着从理论上说明在上述条件下滴定Mg2+的最佳pH=9.6。
在pH=5.0的缓冲溶液中,以2x10^-2mol/L的EDTA滴定相同浓度的Cu2+溶液,欲使终点误差在±0.1%以内。试通过计算说明,能否选用PAN为指示剂。已知:pH=5.0时PAN的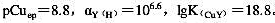 。
。