 更多“已知200℃时五氯化磷分解反应”相关的问题
更多“已知200℃时五氯化磷分解反应”相关的问题
第1题
五氯化磷分解反应为PCl5(g)=PCl3(g)+Cl2(g)。200℃时KΘ=0.312。计算(1)在200℃、200kPa条件下PCl5的解
五氯化磷分解反应为PCl5(g)=PCl3(g)+Cl2(g)。200℃时KΘ=0.312。计算(1)在200℃、200kPa条件下PCl5的解离度;(2)组成为1:5的PCl5和Cl2混合气体在200℃、100kPa条件下PCl5的解离度。
第2题
试以反应式表示乙酸与下列试剂的反应:(1)乙醇(2)三氯化磷(3)五氯化磷(4)氨(5)碱石灰热融
试以反应式表示乙酸与下列试剂的反应:(1)乙醇(2)三氯化磷(3)五氯化磷(4)氨(5)碱石灰热融
点击查看答案
第3题
五氯化磷分解反应为PCl5(g)===PCl3(g)+Cl2(g)。在200℃时的KΘ=0.312,计算:(1)200℃,200kPa下PCl5的解离度;(2)
五氯化磷分解反应为PCl5(g)===PCl3(g)+Cl2(g)。在200℃时的KΘ=0.312,计算:(1)200℃,200kPa下PCl5的解离度;(2)摩尔比为1:5的PCl5与Cl2的混合物,在200 oc,101.325 kPa下,达到化学平衡时PCI5的解离度。
第6题
250℃时,五氯化磷按下式分解: PCl5(g)PCI3(g)+Cl2(g) 将0.700mol的PCl5置于2.00dm3的密闭容器中,达到平衡
250℃时,五氯化磷按下式分解:
PCl5(g)→PCI3(g)+Cl2(g)
将0.700mol的PCl5置于2.00dm3的密闭容器中,达到平衡时有0.200mol分解,试计算该温度下的平衡常数。
第7题
五氯化磷分解反应为PCl5(g)→PCl3(g)+Cl2(g) 已知25℃、下PCl5(g)、PCl3(g)、Cl2(g)的摩尔生成焓分别为-375kJ/m
五氯化磷分解反应为PCl5(g)→PCl3(g)+Cl2(g)
已知25℃、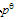 下PCl5(g)、PCl3(g)、Cl2(g)的摩尔生成焓
下PCl5(g)、PCl3(g)、Cl2(g)的摩尔生成焓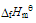 分别为-375kJ/mol、-287kJ/mol、0kJ/mol,摩尔标准熵
分别为-375kJ/mol、-287kJ/mol、0kJ/mol,摩尔标准熵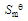 分别为364.6J/(K·mol)、311.8J/(K·mol)、223.07J/(K·mol)。
分别为364.6J/(K·mol)、311.8J/(K·mol)、223.07J/(K·mol)。
第8题
五氧化二磷(PCI3)分解反应在200℃时的K°=0.312,计算:(1)200℃,200kPa下PCI3的解离度;(2)
五氧化二磷(PCI3)分解反应在200℃时的K°=0.312,计算:(1)200℃,200kPa下PCI3的解离度;(2)
点击查看答案
五氧化二磷(PCI3)分解反应
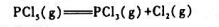
在200℃时的K°=0.312,计算:
(1)200℃,200kPa下PCI3的解离度;
(2)摩尔比为1:5的PCI3与CI2的混合物,在200℃,100kPa下达到平衡时PCI3的解高度.
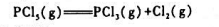

1.jpg)

 如果结果不匹配,请
如果结果不匹配,请 
1.jpg)
















