 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试计算下列化合物已标明键长值的Xe—F键键价。说明稀有气体Xe原子在不同条件下和其他原子形成化学
键的情况。[按(10.1)式计算Xe—F键时,R0值为:Xe2+200pm,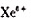 Xe4+193pm,
Xe4+193pm, 189pm;B为37pm]。
189pm;B为37pm]。
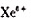 Xe4+193pm,
Xe4+193pm, 189pm;B为37pm]。
189pm;B为37pm]。


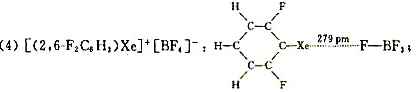
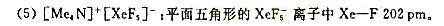
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
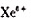 Xe4+193pm,
Xe4+193pm, 189pm;B为37pm]。
189pm;B为37pm]。



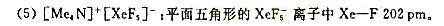
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试计算下列化合物已标明键长值的Xe—F键键价。说明稀有气体X…”相关的问题
更多“试计算下列化合物已标明键长值的Xe—F键键价。说明稀有气体X…”相关的问题
下列关于共价键说法错误的是( )。
(A) 两个原子间键长越短,键越牢固
(B) 两个原子半径之和约等于所形成的共价键键长
(C) 两个原子间键长越长,键越牢固
(D) 键的强度与键长无关
CO2,SO2,NO2,SiO2,BaO2各是什么类型的化合物,指出它们的几何构型;若为分子型化合物,表明有无极性,并说明是怎样由原子形成分子的,分子的各原子间的化学键是σ键还是π键、∏键或配键,若为离子化合物,但其中有共价部分,则也要注明其中的结构。
A.难以描述具有电子离域体系的化合物的结构
B.难以描述含有d电子的原子的成键情况
C.难以描述具有反馈键的化合物的结构
D.难以描述具有配位键的化合物的结构
下列叙述正确的是
(A) 元素原子在化合物中形成共价键的数目等于该基态原子未成对的电子数;
(B) 同核双原子分子双键的键能等于其单键键能的两倍;
(C) 分子内氢键的形成将使该物质的熔点和沸点降低;
(D) 分子的极性只与键的极性有关。