更多“1mol理想气体在恒温下从10L恒温可逆膨胀,若其熵变为5.…”相关的问题
更多“1mol理想气体在恒温下从10L恒温可逆膨胀,若其熵变为5.…”相关的问题
第1题
有1mol某理想气体,体积为V0,做绝热自由膨胀,末态体积为2V0,求该过程熵变为多少?
有1mol某理想气体,体积为V0,做绝热自由膨胀,末态体积为2V0,求该过程熵变为多少?
第2题
1mol双原子分子理想气体在25℃、pθ分别经下列过程到体积增大一倍,求△S、△S环境和△S总。(1)恒温自由膨
1mol双原子分子理想气体在25℃、pθ分别经下列过程到体积增大一倍,求△S、△S环境和△S总。(1)恒温自由膨胀;(2)反抗外压为终态平衡压力(p外p2)恒温膨胀;(3)恒温可逆膨胀;(4)绝热自由膨胀;(5)绝热可逆膨胀。
点击查看答案
第3题
一定量理想气体由同一始态出发,分别经定温可逆膨胀和绝热可逆膨胀到相同终态体积时,终态压力哪个大? (A)
一定量理想气体由同一始态出发,分别经定温可逆膨胀和绝热可逆膨胀到相同终态体积时,终态压力哪个大?
点击查看答案
(A) p恒温>p绝热(B) p恒温<p绝热(C) p恒温=p绝热(D) 无法判断
第4题
1mol理想气体在298K、101.3kPa下等温可逆膨胀,若过程的△G=-2983J,则终态的压力为多少?
1mol理想气体在298K、101.3kPa下等温可逆膨胀,若过程的△G=-2983J,则终态的压力为多少
第6题
0℃时10 dm3氦气He经下列不同途径自106Pa膨胀至终态压力为105Pa,分别计算每一途径的Q、W、△U、△H。假
设氦气为理想气体。 (1)向真空绝热膨胀; (2)在终态压力下恒温、恒外压膨胀; (3)恒温可逆膨胀; (4)绝热可逆膨胀;
点击查看答案
第7题
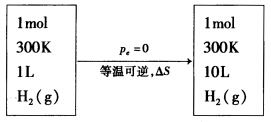
1molH2在300K从体积为1L向真空膨胀至体积为10L,求系统的熵变。若使该H2在300K从1L经等温可逆膨胀至10L其熵变
1molH2在300K从体积为1L向真空膨胀至体积为10L,求系统的熵变。若使该H2在300K从1L经等温可逆膨胀至10L其熵变又是多少?由此得到什么结论?
第8题
理想气体从同一始态(P1,V1)出发,经绝热可逆压缩和恒温可逆压缩,使其终态都达到体积V2,则两过程作的功的绝对值应有()。
A.绝热可逆压缩功大于恒温可逆压缩功
B.绝热可逆压缩功等于恒温可逆压缩功
C.绝热可逆压缩功小于恒温可逆压缩功
D.无确定关系
第9题
1mol单原子理想气体,从始态273K、100kPa,分别经过下列可逆变化到达各自的终态,试计算各过程的Q、W、△U、△H、△S、△
A和△G。已知该气体在273K、100kPa时摩尔熵Sm=100J·mol-1·K-1。
(1)恒温下压力加倍;
(2)恒压下体积加倍;
(3)恒容下压力加倍;
(4)绝热可逆膨胀至压力减少一半;
(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。


 如果结果不匹配,请
如果结果不匹配,请