 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
CO2与H2S在高温下有如下反应:CO2(g)+H2S(g)==COS(g)+H2O(g),今在610K时,将4.4×10-3kg的CO2加入2.
CO2与H2S在高温下有如下反应:CO2(g)+H2S(g)==COS(g)+H2O(g),今在610K时,将4.4×10-3kg的CO2加入2.5dm3体积的空瓶中然后再充入H2S使总压为1000kPa。平衡后水的摩尔分数为0.02。同上试验,在620K,平衡后水的摩尔分数为0.03(计算时可假定气体为理想气体)。 (1)计算610K时的KpΘ。 (2)求610K时的△rGmΘ。 (3)计算反应的热效应△rHmΘ。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“CO2与H2S在高温下有如下反应:CO2(g)+H2S(g)…”相关的问题
更多“CO2与H2S在高温下有如下反应:CO2(g)+H2S(g)…”相关的问题

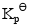 ;
;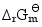 ;
;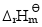 (设其不随温度而变);
(设其不随温度而变);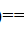 H2O(g)+CO(g)
H2O(g)+CO(g) 今在298K、100kPa下,将Ag放在由等体积的H2和H2S组成的混合气中,
今在298K、100kPa下,将Ag放在由等体积的H2和H2S组成的混合气中,
















