 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知CO的氧化反应及有关热力学数据如下: CO(g) O2(g) CO2(g) Del
已知CO的氧化反应及有关热力学数据如下:、
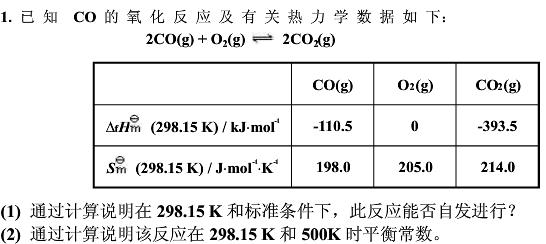
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知CO的氧化反应及有关热力学数据如下:、

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知CO的氧化反应及有关热力学数据如下: CO(g) O2(…”相关的问题
更多“已知CO的氧化反应及有关热力学数据如下: CO(g) O2(…”相关的问题
已知反应在298K的热力学数据如下:CO2(g)+H2=====CO(g)+H2O(g)
2010040 已知反应在298K的热力学数据如下:
CO2(g)+H2=====CO(g)+H2O(g)
ΔfH (kJ·mol-1) -393.5 0 -110.5 -241.8
求:
(1)298K时的反应的焓变;
(2)若此系统在400K时各组分气体的分压为p(CO)=p(H2O)=125kPa,p(CO2)=p(H2)=25kPa,通过计算判断反应进行的方向.已知298K时的平衡常数K=1.25
已知以下反应及有关的热力学数据,计算在298K、标准状态时反应的熵变和焓变,并判断反应能否自发进行。
2SO2(g)+O2(g)====2SO3(g)
在标准状态、298.15K时,利用有关物质的热力学数据计算下列反应的ΔrGm和ΔH,并判断此时的反应方向。
(1)N2(g)+O2(g)→2NO(g);
(2)CO(g)+NO(g)→CO2(g)+1/2N2(g)。
在标准压力和298K时,计算如下反应的,从所得的数值判断反应的可能性。 所需数据自己从热力学数据表上查阅。

已知反应2NO2(g) N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数
N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数 。
。
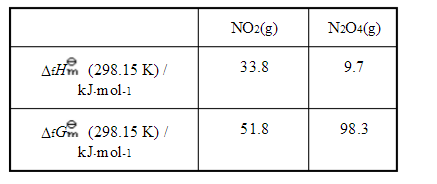
制备半导体材料时发生如下反应,并已知相应热力学数据:
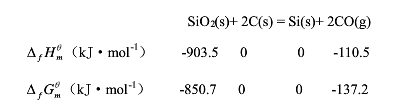
通过计算回答下列问题:
(1)标态下,398.15K时,反应能否自发进行
(2)标态下,反应自发进行的温度
已知下列反应与其相应的热力学数据:
CuS(s)+H2(g)====Cu(s)+H2S(g)
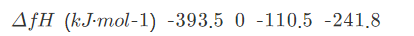
通过计算说明,在标准状态下:
(1)298K时的反应的焓变;
(2)若此系统在400K时各组分气体的分压为p(CO)=p(H2O)=125kPa,p(CO2)=p(H2)=25kPa,通过计算判断反应进行的方向.已知298K时的平衡常数K=1.25
标准反应焓仅是反应物质生成焓的函数,试根据有关物质生成焓的数据,计算气体燃料辛烷C8H18(g)的标准定压热值及标准反应热力学能。