 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
向0.50mol•dm-3的FeCl2溶液通H2S气体至饱和,若控制不析出FeS沉淀,求溶液pH的范围。已知FeS的=6.
向0.50mol•dm-3的FeCl2溶液通H2S气体至饱和,若控制不析出FeS沉淀,求溶液pH的范围。已知FeS的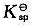 =6.3x10^-18,H2S的
=6.3x10^-18,H2S的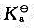 =1.3x10^-20。
=1.3x10^-20。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
向0.50mol•dm-3的FeCl2溶液通H2S气体至饱和,若控制不析出FeS沉淀,求溶液pH的范围。已知FeS的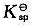 =6.3x10^-18,H2S的
=6.3x10^-18,H2S的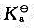 =1.3x10^-20。
=1.3x10^-20。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“向0.50mol•dm-3的FeCl2溶液通H2S气体至饱和…”相关的问题
更多“向0.50mol•dm-3的FeCl2溶液通H2S气体至饱和…”相关的问题
在0.10mol·dm-3Fe2+溶液中通入H2S至饱和(0.10mol·dm-3),欲使Fe2+不生成FeS沉淀,溶液韵pH应是
(已知FeS的 )
)
(A) pH≥2.33; (B) pH≥3.53; (C) pH≤3.53; (D) ph≤2.33。
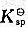 =6.3x10^-18,CuS的
=6.3x10^-18,CuS的 =6.3x10^-36,H2S的
=6.3x10^-36,H2S的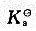 =1.3x10^-20。
=1.3x10^-20。a.先生成CuS沉淀,后生成FeS沉淀;
b.先生成FeS沉淀,后生成CuS沉淀;
c.只生成CuS沉淀,不生成FeS沉淀;
d.只生成FeS沉淀,不生成CuS沉淀。
将H2S气体通入0.1mol·dm-3FeCl2溶液中,达到饱和,问必须控制多大的pH值才能阻止FeS沉淀?
已知向0.010mol·dm-3ZnCl2溶液通H2S至饱和,当溶液的pH=1.0时刚开始有ZnS沉淀产生。若在此浓度ZnCl2溶液中加入1.0mol·dm-3KCN后通入H2S至饱和,求在多大pH时会有ZnS沉淀产生?
{ }
}
在0.1mol·L-1FeCl2溶液中通入H2S,欲使Fe2+不生成FeS沉淀,溶液的pH最高为多少?
某溶液含有FeCl2和CuCl2的浓度均为0.1mol·dm-3,不断通入H2S是否会有FeS沉淀生成?