 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知向0.010mol·dm-3ZnCl2溶液通H2S至饱和,当溶液的pH=1.0时刚开始有ZnS沉淀产生。若在此浓度ZnCl2溶液中加
已知向0.010mol·dm-3ZnCl2溶液通H2S至饱和,当溶液的pH=1.0时刚开始有ZnS沉淀产生。若在此浓度ZnCl2溶液中加入1.0mol·dm-3KCN后通入H2S至饱和,求在多大pH时会有ZnS沉淀产生?
{ }
}
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知向0.010mol·dm-3ZnCl2溶液通H2S至饱和…”相关的问题
更多“已知向0.010mol·dm-3ZnCl2溶液通H2S至饱和…”相关的问题
 (ZnS)=2.0×10-22,
(ZnS)=2.0×10-22,

 =6.3x10^-18,H2S的
=6.3x10^-18,H2S的 =1.3x10^-20。
=1.3x10^-20。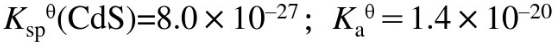 。
。















