 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol单原子分子理想气体自2×105Pa、0℃经两个不同的途径变到105Pa、50℃。分别计算两个途径的Q、W、△U和
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“1mol单原子分子理想气体自2×105Pa、0℃经两个不同的…”相关的问题
更多“1mol单原子分子理想气体自2×105Pa、0℃经两个不同的…”相关的问题
1mol单原子理想气体,从始态(273K、200kPa)到终态(323K、100kPa),通过两个途径:(1)先等压加热至323K,再等温可逆膨胀至100kPa;(2)先等温可逆膨胀至100kPa,再等压加热至323K。请分别计算两个途径的Q、W、△U和△H,试比较两种结果有何不同,并说明原因。
始态为T1=300K,P1=200kPa的某双原子理想气体1mol,经两条不同途径变化到T2=300K,P2=100kPa的末态。求各步的Q、△S。

1mol单原子理想气体,始态为p1=202650Pa,T1=273K,沿可逆途径p/V=K(K是常数)至终态,压力增加一倍。(1)计算V1、V2、T2、Q、W、△U、△H;(2)计算该气体沿此途径的热容C。
1mol单原子理想气体从273K,202.65kPa,经pT=C的可逆途径压缩到405.3kPa的终态,该气体的△U为
(A) 1702J (B) -406.8J (C) 406.8J (D) -1702J
1mol单原子分子理想气体,在273.2K、1.0×105Pa时发生一变化过程,体积增大一倍,Q=1674J,△H=2092J。
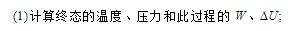

。画出p-V示意图,并把△U和W,值按大小次序排列。
(1)等温可逆膨胀;
(2)绝热可逆膨胀;
(3)沿着p/Pa=1.0×104Vm/(dm3·mol-1)+b的途径可逆变化。
1mol单原子理想气体,由温度为273K,体积为22.4dm3的始态,经由Ⅰ途径变化到温度为546K、体积仍为22.4dm3;再经由Ⅱ途径定温可逆膨胀至体积为44.8dm3;最后经由Ⅲ途径使系统定压回到其初态。试求出:
(1) 各状态下的气体压力;
(2) 系统经由各途径时的Q,W,△U,△H;
(3) 该循环过程的Q,W,△U,△H。
A.1702J
B.-406.8J
C.406.8J
D.-1702J
始态为T1=300K,P1=200kPa的某双原子理想气体1mol,经下列不同途径变化到T2=300K,P2=100kPa的末态。求各步骤及途径的Q,△S。
(1)恒温可逆膨胀;(2)先恒容冷却至使压力降至100kPa,再恒压加热至T2;(3)先绝热可逆膨胀到使压力降至100kPa,再恒压加热至T2。