 更多“计算各原电池在298.15K时的标准电动势和各电池反应的标准…”相关的问题
更多“计算各原电池在298.15K时的标准电动势和各电池反应的标准…”相关的问题
8.在298.15K时,有下列反应
H3AsO4+2I-+2H+====H3AsO3+I2+H2O
(1) 计算该反应组成的原电池的标准电动势。
(2) 计算该反应的标准摩尔吉布斯自由能变并指出该反应能否自发进行。
(3) 若溶液的的pH=7,而c(H3AsO4)=c(H3AsO3)=c(I-)=1mol·dm-3此反应的△rGm是多少?此时反应进行方向?
将反应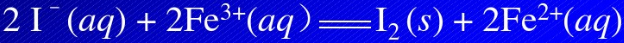 组成原电池(温度为298.15K):(1)计算原电池的标准电动势;(2)计算反应的标准摩尔吉布斯函数变;(3)用图式表示原电池;(4)计算c(I-)=1.0×10-2mol·dm-3以及c(Fe3+)=c(Fe2+)/10时原电池的电动势。
组成原电池(温度为298.15K):(1)计算原电池的标准电动势;(2)计算反应的标准摩尔吉布斯函数变;(3)用图式表示原电池;(4)计算c(I-)=1.0×10-2mol·dm-3以及c(Fe3+)=c(Fe2+)/10时原电池的电动势。
写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势、各电池反应的摩尔吉布斯函数变及标准平衡常数,并指明各电池反应能否自发进行。
(1)Cd|Cd2+{a(Cd2+)=0.01}||Cl-{a(Cl-)=0.5}|Cl2(g,100kPa)|Pt
(2)Pb|Pb2+{a(Pb2+)=1}||Ag+{a(Ag+)=1}|Ag
(3)Zn|Zn2+{a(Zn2+)=0.0004}||Cd2+{a(Cd2+)=0.2}|Cd
已知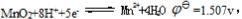 Fe3++e-===Fe2+EΘ=0.771V
Fe3++e-===Fe2+EΘ=0.771V
(1)判断下列反应的方向,并配平
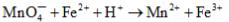
(2)将这两个半电池组成原电池,用电池符号表示该原电池的组成,标明电池的正、负极,并计算其标准电动势。
(3)当氢离子浓度为10mol·L-1,其他各离子浓度均为1mol·L-1时,计算该电池的电动势。
写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势及电池反应的摩尔吉布斯函数变,并指明各电池反应能否自发进行。
(1)Pt|H2(g,100kPa)|HCl[a(HCl)=1]|Cl2(g,100kPa)|Pt
(2)Zn|ZnCl2[a(ZnCl2)=0.5]|AgCl(S)|Ag
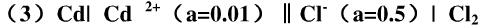
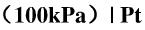
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
(1)电池Pt|H2(PH2) |NaOH(a) |HgO(s) |Hg(I)的标准电动势 =0.9265V;
=0.9265V;
(2)反应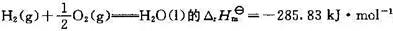 ;
;
(3)298K时,下表为各物质的标准摩尔熵值:

试以中和反应H+(ag)+OH-(ag)====H2O(l)为电池反应,设计一种原电池(用电池符号表示)。分别写出电极半反应,并计算25℃时标准电动势。


 如果结果不匹配,请
如果结果不匹配,请 
















