 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应时间与转化率 氧化亚氮的分解反应可按二级速率方程进行 2N2O→2N2+O2 在895℃时正反应速率常数k为977c
反应时间与转化率
氧化亚氮的分解反应可按二级速率方程进行
2N2O→2N2+O2
在895℃时正反应速率常数k为977cm3/(mol·s),逆反应速率可以忽略。初始压力为0.10133MPa,反应开始时反应器中全为N2O。试计算在间歇反应器中时间为1.0s、10s及10min时的分解率。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“反应时间与转化率 氧化亚氮的分解反应可按二级速率方程进行 2…”相关的问题
更多“反应时间与转化率 氧化亚氮的分解反应可按二级速率方程进行 2…”相关的问题

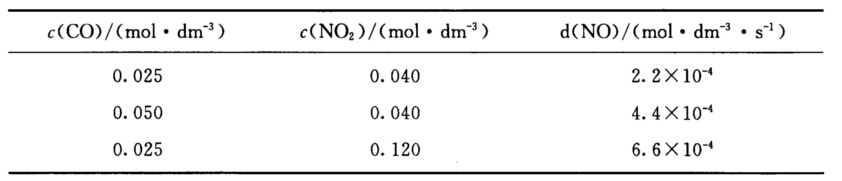 (1)写出反应的速率方程; (2)求650 K时的速率常数; (3)当c(CO)=0.10 mol.dm-3,c(NO2)=0.16 mol.dm-3时,求650 K时的反应速率; (4)若800 K时速率常数为23.0 dm3mol-1.s-1,求反应的活化能。
(1)写出反应的速率方程; (2)求650 K时的速率常数; (3)当c(CO)=0.10 mol.dm-3,c(NO2)=0.16 mol.dm-3时,求650 K时的反应速率; (4)若800 K时速率常数为23.0 dm3mol-1.s-1,求反应的活化能。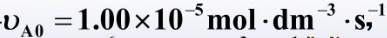 ,1小时后,速率r=3.26×10-6mol·dm-3·s-1,试求:(1) 反应速率常数;(2) 半衰期t1/2;(3) 初始浓度。
,1小时后,速率r=3.26×10-6mol·dm-3·s-1,试求:(1) 反应速率常数;(2) 半衰期t1/2;(3) 初始浓度。















