 更多“中和滴定时,滴至等当点的PH值为7。()”相关的问题
更多“中和滴定时,滴至等当点的PH值为7。()”相关的问题
第1题
有一三元酸,其。用氢氧化钠溶液滴定时,第一和第二化学计量点的pH分别为多少?两个化学计量点附近有无pH突跃?
有一三元酸,其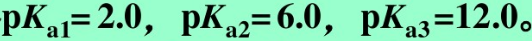 用氢氧化钠溶液滴定时,第一和第二化学计量点的pH分别为多少?两个化学计量点附近有无pH突跃?可选用什么指示剂?能否直接滴定至酸的质子全部被作用?
用氢氧化钠溶液滴定时,第一和第二化学计量点的pH分别为多少?两个化学计量点附近有无pH突跃?可选用什么指示剂?能否直接滴定至酸的质子全部被作用?
第2题
某弱酸,现有其共轭碱NaA溶液20.00mL,浓度为0.10mol·L-1,当用0.10moI·L-1HCl溶液滴定时,化学计量点的pH为多
某弱酸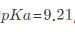 ,现有其共轭碱NaA溶液20.00mL,浓度为0.10mol·L-1,当用0.10moI·L-1HCl溶液滴定时,化学计量点的pH为多少?化学计量点附近的pH突跃为多少?
,现有其共轭碱NaA溶液20.00mL,浓度为0.10mol·L-1,当用0.10moI·L-1HCl溶液滴定时,化学计量点的pH为多少?化学计量点附近的pH突跃为多少?
第3题
以0.100mol•L-1的NaOH溶液滴定0.100mol•L-1某二元弱酸H2A溶液,已知当滴定至pH=1.92时,[H2A]=[HA-],滴定至pH=6.22时,[HA-]=[A2-]。计算:(1)中和至第一化学计量点时,溶液的pH值为多少?选用何种指示剂为宜?(2)中和至第二化学计量点时,溶液的pH值为多少?选用何种指示剂为宜?
第4题
用浓度为cEDTA=0.0500mol·dm-3的溶液滴定100.0cm3浓度为的Zn2+,滴定开始时,pH=5.50,若溶液中无缓冲溶液,滴
用浓度为cEDTA=0.0500mol·dm-3的溶液滴定100.0cm3浓度为的Zn2+,滴定开始时,pH=5.50,若溶液中无缓冲溶液,滴定至终点时,溶液的pH值为多少?通过计算说明EDTA配位滴定时加入缓冲溶液的必要性。
第6题
锥形瓶中盛放20mL、0.10mol·L-1NH3溶液,现以0.10mol·L-1HCl滴定之。试计算: (1)当滴入20mL HCl后,混合液的pH值;
锥形瓶中盛放20mL、0.10mol·L-1NH3溶液,现以0.10mol·L-1HCl滴定之。试计算:
(1)当滴入20mL HCl后,混合液的pH值;
(2)当滴入30mL HCl后,混合液的pH值。
第7题
取1.25 g一元弱酸溶解于50.00 mL水中,用浓度为0.090 00 mol·L-1的NaOH标准溶液滴定,滴定至化学计
量点时,耗去41.20 mL。求: (1)一元弱酸的相对分子质量为多少? (2)滴定时,当加入NaOH溶液8.24 mL时,溶液的pH值为4.30,求一元弱酸的Ka值。 (3)计算化学计量点时的pH值。 (4)滴定应使用何种指示剂?
点击查看答案
第9题
有0.20mol·L-1二元弱酸H2B溶液30.00mL,滴入0.20mol·L-1NaOH溶液15.00mL时的pH=4.70,当滴入30.00mLNaOH时,达
有0.20mol·L-1二元弱酸H2B溶液30.00mL,滴入0.20mol·L-1NaOH溶液15.00mL时的pH=4.70,当滴入30.00mLNaOH时,达到第一化学计量点的pH=7.20,则H2B的是多少?
第11题
下列氨基酸测定操作错误的是()。
A.用标准缓冲溶液pH为6.86和9.18的校正酸度计
B.用NaOH溶液准确地中和样品中的游离酸
C.应加入10mL甲酸溶液
D.用NaOH标准溶液滴至pH为9.20


 如果结果不匹配,请
如果结果不匹配,请 
















