 更多“丁二烯气相二聚反应,反应速率常数k为”相关的问题
更多“丁二烯气相二聚反应,反应速率常数k为”相关的问题
第1题
丁二烯气相二聚反应,反应速率常数k为(1)用过渡态理论计算该反应在600 K时的指前因子,已知 。(
丁二烯气相二聚反应,反应速率常数k为
点击查看答案
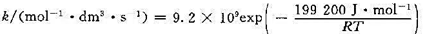
(1)用过渡态理论计算该反应在600 K时的指前因子,已知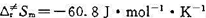 。
。
(2)若有效碰撞直径d=0.5nm,用简单的碰撞理论计算该反应的指前因子;
(3)通过计算讨论概率因子P与活化熵 的关系。
的关系。
第2题
已知某气相反应的活化能Ea=163kJ·mol-1,温度390K时的速率常数k=2.37×10-2dm3·mol-1·s-1。试求温度为420K时的
已知某气相反应的活化能Ea=163kJ·mol-1,温度390K时的速率常数k=2.37×10-2dm3·mol-1·s-1。试求温度为420K时的反应速率常数。
第4题
有恒容气相反应A(g)→D(g),已知该反应的速率常数k与温度T有关系:lnk(s-1)=24.00-9622/T(K)
有恒容气相反应A(g)→D(g),已知该反应的速率常数k与温度T有关系:lnk(s-1)=24.00-9622/T(K)
点击查看答案
第6题
速率常数的变换 在400K之下,某气相反应速率表达式为: 问: (1)速率常数的单位是什么? (2)如速率方程式
速率常数的变换
在400K之下,某气相反应速率表达式为:
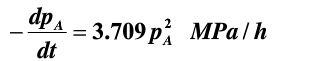
问:
(1)速率常数的单位是什么?
(2)如速率方程式表达为
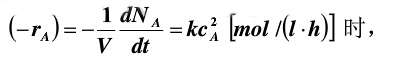
速率常数等于多少?
第7题
已知65℃时N2O5气相分解反应速率常数的单位是min-1,半衰期为2.37min,反应的活化能为103.3kJ·mol-1,求80℃时的
已知65℃时N2O5气相分解反应速率常数的单位是min-1,半衰期为2.37min,反应的活化能为103.3kJ·mol-1,求80℃时的速率常数。
第8题
反应A+B→C的反应速率方程式为v=k[C(A)]1/2c(B),当A的浓度增大时,反应速率将______,反应速率常数k将______。
反应A+B→C的反应速率方程式为v=k[C(A)]1/2c(B),当A的浓度增大时,反应速率将______,反应速率常数k将______。升高温度时,反应速率常数将______,反应速率将______。
点击查看答案
第9题
气相反应2A→P+2S,反应在理想管式反应器中进行,压力为0.1MPa,温度为700℃,已知反应为一级反应,反应速率常数k=
0.97s-1,如进料衡分子流率FA0=0.4kmol/min,转化率xA=0.8,试计算反应器体积。
点击查看答案



 如果结果不匹配,请
如果结果不匹配,请 
















