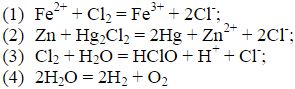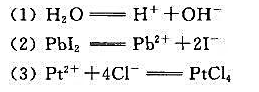更多“用图式表示反应可能组成的原电池,并利用标准电极电势数据计算反…”相关的问题
更多“用图式表示反应可能组成的原电池,并利用标准电极电势数据计算反…”相关的问题
第1题
将反应组成原电池(温度为298.15K):(1)计算原电池的标准电动势;(2)计算反应的标准摩尔吉布斯函数变;(3)用图
将反应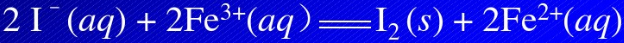 组成原电池(温度为298.15K):(1)计算原电池的标准电动势;(2)计算反应的标准摩尔吉布斯函数变;(3)用图式表示原电池;(4)计算c(I-)=1.0×10-2mol·dm-3以及c(Fe3+)=c(Fe2+)/10时原电池的电动势。
组成原电池(温度为298.15K):(1)计算原电池的标准电动势;(2)计算反应的标准摩尔吉布斯函数变;(3)用图式表示原电池;(4)计算c(I-)=1.0×10-2mol·dm-3以及c(Fe3+)=c(Fe2+)/10时原电池的电动势。
第2题
将下列氧化还原反应设计成为两个半电池反应,并利用标准电极电势表的数据,求出298K时反应的平衡常数。
将下列氧化还原反应设计成为两个半电池反应,并利用标准电极电势表的数据,求出298K时反应的平衡常数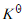 。
。
第4题
将反应2I-(aq)+2Fe3+=I2(s)+2Fe3+(aq)组成原电池(温度为298.15 K): (1)计算原电池的标准电动势;
将反应2I-(aq)+2Fe3+=I2(s)+2Fe3+(aq)组成原电池(温度为298.15 K): (1)计算原电池的标准电动势; (2)计算反应的标准摩尔吉布斯函数变; (3)用图式表示原电池; (4)计算c(I-)=1.0×10-2mol.dm-3以及c(Fe3+)=c(Fe2+)/10时原电池的电动势。
点击查看答案
第7题
298K时,已知,试计算:(1)反应Hg2++2e→Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计
298K时,已知
点击查看答案
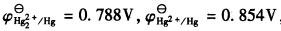 ,试计算:(1)反应Hg2++2e→
,试计算:(1)反应Hg2++2e→
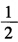 Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
第8题
将标准Ag-AgCl电极与饱和甘汞电极组成原电池,该原电池的电池符号______;正极反应______;负极反应______;电
将标准Ag-AgCl电极Eθ(AgCl/Ag)=0.2222V与饱和甘汞电极Eθ=0.2145V组成原电池,该原电池的电池符号______;正极反应______;负极反应______;电池反应______;电池反应的平衡常数______。
第9题
已知下列标准电极电势 Cu2++2e-===Cu EΘ=0.337V Cu2++e-===Cu+ EΘ=0.153V (1)计算反应Cu+Cu2+===2
已知下列标准电极电势
Cu2++2e-===Cu EΘ=0.337V
Cu2++e-===Cu+EΘ=0.153V
(1)计算反应Cu+Cu2+===2Cu+的平衡常数。
(2)已知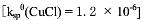 ,试计算下面反应的平衡常数。
,试计算下面反应的平衡常数。
Cu+Cu2++2Cl=2CuCl↓

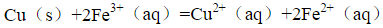

 如果结果不匹配,请
如果结果不匹配,请