 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在SO2,氧化成SO2,反应的某一时刻,SO2的反应速率为13.60mol·L-1·h-1,试求这时SO2和SO2的反应速率各是多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在SO2,氧化成SO2,反应的某一时刻,SO2的反应速率为1…”相关的问题
更多“在SO2,氧化成SO2,反应的某一时刻,SO2的反应速率为1…”相关的问题
0.1013MPa压力下,在钒催化剂上进行SO2氧化反应,原料气组成(摩尔分数)为SO27%,O211%和N282%。试计算SO2转化率为80%时的最佳温度。SO2在钒催化剂上氧化的正反应活化能为9.211×104J/mol,化学计量数为1/2,反应式为

该反应的热效应△Hr=-9.629×105J/mol。
已知可逆反应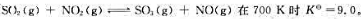 若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
A、2dc(SO3)/dt
B、-dc(SO2)/2dt
C、-2dc(SO2)/dt
D、-dc(SO2)/dt
试求293K下,混合气体中SO2平衡分压为0.05atm时,SO2在水中的溶解度。已知293K下
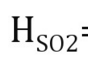 为1.63kmol/(atm·m3),离解常数
为1.63kmol/(atm·m3),离解常数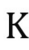 为:
为: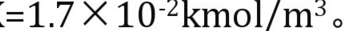
实验测得SO2氧化为SO3的反应,在1000K时,各物质的平衡分压为p(SO2)=27.7kPa、p(O2)=40.7kPa、p(SO3)=32.9kPa。计算该温度下反应2SO2(g)+O2(g)====2SO3(g)的平衡常数Kp。
已知反应2SO2+O2====2SO3在1062K时的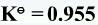 ,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
已知反应2SO2+O2=2SO3,在1062K时的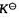 =0.955,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,p(O2)= 60.1kPa, p(SO3)=25.3kPa。试判断反应进行的方向。
=0.955,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,p(O2)= 60.1kPa, p(SO3)=25.3kPa。试判断反应进行的方向。
,O2的起始浓度为2mol/L,SO2的平衡转化率为25%,求平衡时反应混合物中SO3的体积分数。若将O2的起始浓度加大至4mol/L,SO2的起始浓度不变,平衡时测得SO3的浓度为2.8mol/L,求SO2、O2各自的转化率
反应SO2(g)+1/2O2(g)=SO2(g)的标准吉布斯自由能变与温度的关系为ΔrGmθ=(-94500+89.50T/K)Jmol-1.若反应起始时系统中含SO2为6%(摩尔分数,下同),含O2为12%,则在标准压力下,欲使SO2的中衡转化率达90%,反应温度应控制为若干?
用清水在吸收塔中逆流吸收混合气中的SO2,混合气流量为5000标准m3/h,其中含SO2的摩尔比为0.1,要求SO2回收率为95%,操作条件的气一液相平衡为Y*=2.7X,试求: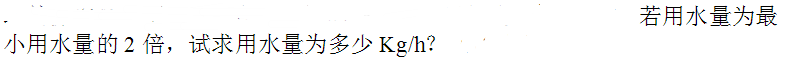
SO2转化成SO3的反应:SO2+0.5O2=SO3,平衡常数KP=20.0,系统恒压为1.00MPa,
4.00molSO2与2.00molO2混合,求平衡时SO2的转化率。(平衡时SO3约为3.3~3.5mol)