 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
水煤气的反应方程为 CO+H2O→CO2+H2试根据平衡常数的定义表达式,计算温度为1000K时水煤气反应的平衡常数。
水煤气的反应方程为 CO+H2O→CO2+H2试根据平衡常数的定义表达式,计算温度为1000K时水煤气反应的平衡常数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
水煤气的反应方程为 CO+H2O→CO2+H2试根据平衡常数的定义表达式,计算温度为1000K时水煤气反应的平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“水煤气的反应方程为 CO+H2O→CO2+H2试根据平衡常数…”相关的问题
更多“水煤气的反应方程为 CO+H2O→CO2+H2试根据平衡常数…”相关的问题
在高温下水蒸气通过灼热的煤层,按下式生成水煤气:
C(石墨)+H2O(g)===H2(g)+CO(g)
若在1000K及1200K时,KΘ分别为2.472及37.58,试计算此温度范围内的平均摩尔反应焓△rHm,及1100K时反应的标准平衡常数KΘ。
已知反应2NO2(g)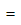 N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数
N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数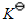 。
。
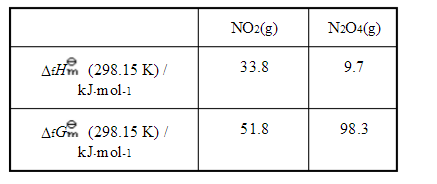
 (1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
(1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
实验测得SO2氧化为SO3的反应,在1000K时,各物质的平衡分压为p(SO2)=27.7kPa、p(O2)=40.7kPa、p(SO3)=32.9kPa。计算该温度下反应2SO2(g)+O2(g)====2SO3(g)的平衡常数Kp。