 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
气相反应2SO2+O2=2SO3,反应的某一时刻O2的消耗速率为6.36mol·dm-3·h-1.此时SO2的消耗速率、SO3的生成速率和该反应的反应速率各为何值?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“气相反应2SO2+O2=2SO3,反应的某一时刻O2的消耗速…”相关的问题
更多“气相反应2SO2+O2=2SO3,反应的某一时刻O2的消耗速…”相关的问题
在660K时,反应
2NO(g)+O2(g)→2NO2(g)
的实验数据如下:
初始浓度/(mol·L-1) | 初始速率/(mol·L-1·s-1) (NO消耗速率) | |
c(NO) | c(O2) | |
0.010 | 0.010 | 2.5×10-3 |
0.010 | 0.020 | 5.0×10-3 |
0.030 | 0.020 | 45×10-3 |
(1)写出该反应的速率方程式,该反应的反应级数是多少?
(2)计算速率常数。
(3)当c(NO)=0.015mol·L-1,c(O2)=0.025mol·L-1时,反应速率为多少?
A.滴定过程中消耗H+,使反应速率加快
B.滴定过程中产生H+,使反应速率加快
C.滴定过程中反应物浓度越来越小,使反应速率越来越快
D.反应产生Mn2+,它是KMnO4与H2O2反应的催化剂
E.反应产生O2,使反应速率加快
生成速率表示):
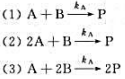
对基元反应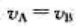 反应物A的消耗速率vA与反应物B的消耗速率vB的关系为()
反应物A的消耗速率vA与反应物B的消耗速率vB的关系为()
A、
B、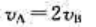
C、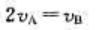
D、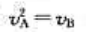
A、2dc(SO3)/dt
B、-dc(SO2)/2dt
C、-2dc(SO2)/dt
D、-dc(SO2)/dt
气相反应4A→Y+6Z的反应速率常数kA与温度的关系为: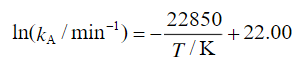 ,且反应速率与产物浓度无关。求:
,且反应速率与产物浓度无关。求:
速率常数的变换
在400K之下,某气相反应速率表达式为:

问:
(1)速率常数的单位是什么?
(2)如速率方程式表达为
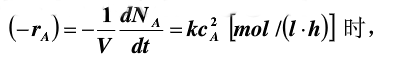
速率常数等于多少?