 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在真空的容器中放入固态的NH4HS,于25℃下分解为NH3(g)与H2S(g),平衡时容器内的压力为66.66kPa。(1)当放入NH4H
在真空的容器中放入固态的NH4HS,于25℃下分解为NH3(g)与H2S(g),平衡时容器内的压力为66.66kPa。(1)当放入NH4HS时容器内已有39.99kPa的H2S(g),求平衡时容器中的压力;(2)容器内原有6.666kPa的NH3(g),问需加多大压力的H2S,才能形成NH4HS。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在真空的容器中放入固态的NH4HS,于25℃下分解为NH3(…”相关的问题
更多“在真空的容器中放入固态的NH4HS,于25℃下分解为NH3(…”相关的问题


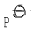 ,则标准平衡常数为
,则标准平衡常数为
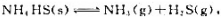 指出下列各系统的独立组分数和白由度数.
指出下列各系统的独立组分数和白由度数.















