 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298 K时,以石墨为阳极,电解0.01 mol·kg-1NaCl溶液,已知 =1.36V, =0V, =0.401V, =0.8V,则在阳极
A. Cl2
B.O2
C. Cl2与O2混合气体
D.无气体析出
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A. Cl2
B.O2
C. Cl2与O2混合气体
D.无气体析出
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298 K时,以石墨为阳极,电解0.01 mol·kg-1N…”相关的问题
更多“298 K时,以石墨为阳极,电解0.01 mol·kg-1N…”相关的问题
 =1.36V,
=1.36V,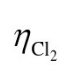 =0V,
=0V,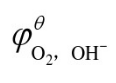 =0.401V,
=0.401V,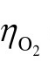 =0.8V,则在阳极上首先析出( )
=0.8V,则在阳极上首先析出( )A.Cl2
B.O2
C.Cl2与O2混合气体
D.元气体析出
电解NiSO4溶液,阳极用镍,阴极用铁,则阴、阳极的电解产物分别为______和______;电解熔融MgCl2,阳极用石墨,阴极用铁,则阴、阳极的电解产物分别为______和______。
在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中超电势可忽略不计, (设活度因子均为1),试问:
(设活度因子均为1),试问:

l·kg-1的FeCl2水溶液.请试求:
(1)哪种离子优先在阴极上析出?
(2)当第二种金属析出时,第一种金属离子在溶液中的浓度为多少?
(3)若氧气和氧气在Pt上的超电势分别为0.900V和0.200V,当第二种离子析出时,则阳极上首先应发生什么反应?此时外加电压至少为多少?
试用反应式表示下列电解过程中的主要电解产物。 (1)电解NiSO4溶液,阳极用镍,阴极用铁。 (2)电解熔融MgCl2,阳极用石墨,阴极用铁。 (3)电解KOH溶液,两极都用铂。
在298K和标准压力下,用铁Fe(s)为阴极,C(石墨)为阳极,电解6.0mol·kg-1的NaCl水溶液。若H2(g)在铁阴极上的超电势为0.20V,O2(g)在石墨阳极上的超电势为0.60V,Cl2(g)的超电势可忽略不计,试说明两极上首先发生的反应及计算至少需加多少外加电压,电解才能进行(设活度因子均为1)。
298K、100kPa时,用Pb(s)电极电解H2SO4溶液(m=0.10mol/kg,γ±=0.265)。若在电解过程中,把Pb电极作为阴极,甘汞电极(cKCl=1mol/L)作为阳极组成原电池,测得其电动势E为1.0685V。试求H2(100kPa)在铅电极上的超电势(只考虑H2SO4一级电离)。已知
在298K时,用Pb(s)作电极电解Pb(NO3)2溶液,该溶液的浓度为每1000g水中含有Pb(N03)216.64g,当与电解池串联的银库仑计中有0.1658g银沉积时就停止通电。已知阳极部溶液质量为62.50g,经分析含有Pb(NO3)21.151g,计算Pb2+的迁移数。
在锌电极上析出氢气的Tafel公式为
η/V=0.72+0.116lg[j/(A·cm-2)]
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?