 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列热力学数据(T=298K)计算说明,要使Ag2CO3(s)=Ag2O(s)+CO2(g)分解反应在大气环境下(大气中
已知下列热力学数据(T=298K)
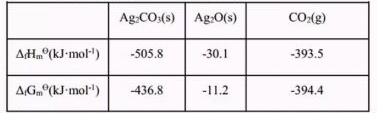
计算说明,要使Ag2CO3(s)=Ag2O(s)+CO2(g)分解反应在大气环境下(大气中CO2分压为30Pa)能自发进行,温度必须高于多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列热力学数据(T=298K)

计算说明,要使Ag2CO3(s)=Ag2O(s)+CO2(g)分解反应在大气环境下(大气中CO2分压为30Pa)能自发进行,温度必须高于多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知下列热力学数据(T=298K)计算说明,要使Ag2CO3…”相关的问题
更多“已知下列热力学数据(T=298K)计算说明,要使Ag2CO3…”相关的问题
通过计算说明在298.15K、标准压力下,用C还原Fe2O3生成Fe和CO2在热力学上是否可能?若要反应自发进行,温度最低为多少?已知298.15K时相关热力学数据如下:
3C(石墨)+2Fe2O3(s)====4Fe(s)+3CO2(g)

已知反应在298K的热力学数据如下:CO2(g)+H2=====CO(g)+H2O(g)
2010040 已知反应在298K的热力学数据如下:
CO2(g)+H2=====CO(g)+H2O(g)
ΔfH (kJ·mol-1) -393.5 0 -110.5 -241.8
求:
(1)298K时的反应的焓变;
(2)若此系统在400K时各组分气体的分压为p(CO)=p(H2O)=125kPa,p(CO2)=p(H2)=25kPa,通过计算判断反应进行的方向.已知298K时的平衡常数K=1.25
制备半导体材料时发生如下反应,并已知相应热力学数据:
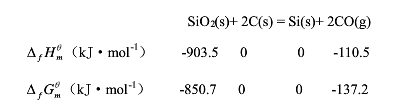
通过计算回答下列问题:
(1)标态下,398.15K时,反应能否自发进行
(2)标态下,反应自发进行的温度
Ag2CO3在110℃的空气流中干燥,为防止Ag2CO3分解,空气中CO2的分压至少应为多少?有关热力学数据如下:

Ag2CO3(s) -505.8 167.4
Ag2O(s) -31.1 121.3
CO2(g) -393.5 213.8
利用热力学数据计算5题中反应在298.15K时的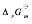 ,并判断在标准状态下该反应能否自发进行?
,并判断在标准状态下该反应能否自发进行?

CaCO3(s)===CaO(s)+CO2(g)
已知,
,假定反应的
不随温度的变化而变化,计算CaCO3的最低分解温度和该温度下CO2的分压是多少?
①
,
②
,
通过计算说明反应:CaO(s)+CO2(g)====CaCO3(s)在标准状态时能自发进行的温度是多少?